
| A. | 1 mol H2O所含电子数为10NA | |
| B. | 1 mol Al与足量的稀盐酸溶液反应生成氢气1.5 mol | |
| C. | 在标准状况下,0.5NA Cl2所占的体积约是11.2 L | |
| D. | 在非标准状况下,22.4 L O2含有的分子数一定不是NA |
分析 A、水为10电子微粒;
B、1mol铝反应后失去3mol电子;
C、气体体积V=$\frac{N}{{N}_{A}}Vm$;
D、在非标况下,气体摩尔体积也可能为22.4L/mol.
解答 解:A、水为10电子微粒,故1mol水中含10NA个电子,故A正确;
B、1mol铝反应后失去3mol电子,故能将3mol氢离子还原为1.5mol氢气,故B正确;
C、气体体积V=$\frac{N}{{N}_{A}}Vm$=$\frac{0.5{N}_{A}}{{N}_{A}/mol}×22.4L/mol$=11.2L,故C正确;
D、在非标况下,气体摩尔体积也可能为22.4L/mol,故22.4L氧气的物质的量可能为1mol,则含有的分子个数可能为NA个,故D错误.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
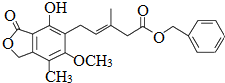 ,下列关于该化合物的说法不正确的是( )
,下列关于该化合物的说法不正确的是( )| A. | 该有机物的分子式为C23H24O6 | |
| B. | 1mol该化合物最多可以与9molH2发生加成反应 | |
| C. | 既可以使溴的四氯化碳溶液褪色,又可以使酸性KMnO4溶液褪色 | |
| D. | 既可以与FeCl3溶液发生显色反应,又可以与Na2CO3溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgO、H2SO4、Na2O、CaCl2 | B. | MnO2、HNO3、KOH、K2CO3 | ||
| C. | SO2、NaHSO4、Ca(OH)2、KCl | D. | H2O、HCl、纯碱(Na2CO3)、盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
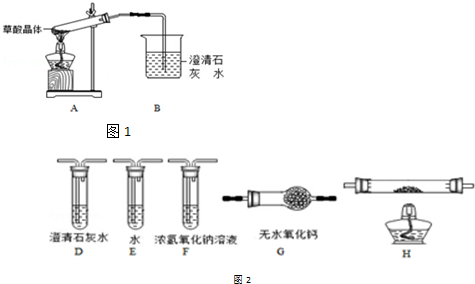
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
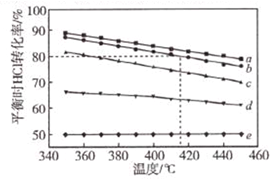 文献报道:利用氯化氢氧化反应一脱水耦合工艺,可用有机氯化工艺的副产品氯化氢为原料制备氯气,实现氯的循环利用,原理为4HCl(g)+O2(g)?2Cl2(g)+2H2O(g).将HC1和O2分别以5种物质的量比:①1:1 ②2:1 ③4:1 ④6:1 ⑤8:1,向五个容积可变的容器中投料时,反应温度对HCl平衡转化氯影响的曲线如图.
文献报道:利用氯化氢氧化反应一脱水耦合工艺,可用有机氯化工艺的副产品氯化氢为原料制备氯气,实现氯的循环利用,原理为4HCl(g)+O2(g)?2Cl2(g)+2H2O(g).将HC1和O2分别以5种物质的量比:①1:1 ②2:1 ③4:1 ④6:1 ⑤8:1,向五个容积可变的容器中投料时,反应温度对HCl平衡转化氯影响的曲线如图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH试纸测试 | B. | 用闻气味和pH试纸测试 | ||
| C. | 用Ba(OH)2溶液和酚酞试液 | D. | 用NaOH和BaCl2溶液鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com