
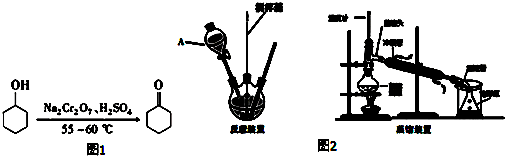
| 名称 | 性状 | 密度 | 溶点℃ | 沸点℃ | 溶解度 | |
| 水 | 乙醚 | |||||
| 环已醇 | 无色,有刺激性气味 | 0.9624 | 25.93 | 161.5 | 5.67g/100mL | ∞ |
| 环已酮 | 无色,有刺激性气味 | 0.9478 | - | 155.7 | 2.4g/100mL | ∞ |
 +1 Na2Cr2O7+4H2SO4→3
+1 Na2Cr2O7+4H2SO4→3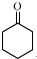 +1 Na2SO4+1 Cr2(SO4)3+7 H2O
+1 Na2SO4+1 Cr2(SO4)3+7 H2O分析 (1)装置A为分液漏斗;
(2)环己醇转变为环己酮C的化合价升高2价,而Na2Cr2O7中Cr元素化合价由+6价降低为+3价,降低3×2=6价,化合价升降最小公倍数为6,据此确定环己醇、Na2Cr2O7系数,再根据原子守恒配平方程式;
(3)根据甲醇具有还原性,与过量的重铬酸钠发生氧化还原反应生成二氧化碳、Cr3+和H2O,防止环己酮继续被过量的重铬酸钠氧化;
(4)环己酮在氯化钠中的溶解度较小;根据乙醚提取液中含有少量的环己酮分析;
(5)根据反应3 +1Na2Cr2O7+4H2SO4→3
+1Na2Cr2O7+4H2SO4→3 +1Na2SO4+1 Cr2(SO4)3+7H2O计算出理论上生成环己酮的质量,再利用产率=$\frac{实际值}{理论值}$×100%计算.
+1Na2SO4+1 Cr2(SO4)3+7H2O计算出理论上生成环己酮的质量,再利用产率=$\frac{实际值}{理论值}$×100%计算.
解答 解:(1)装置A为分液漏斗,故答案为:分液漏斗;
(2)环己醇转变为环己酮C的化合价升高2价,而Na2Cr2O7中Cr元素化合价由+6价降低为+3价,降低3×2=6价,化合价升降最小公倍数为6,可知环己醇、Na2Cr2O7系数3、1,再根据原子守恒配平方程式为3 +1Na2Cr2O7+4H2SO4→3
+1Na2Cr2O7+4H2SO4→3 +1Na2SO4+1 Cr2(SO4)3+7H2O,
+1Na2SO4+1 Cr2(SO4)3+7H2O,
故答案为:3,1,4,3,1,1,7;
(3)甲醇具有还原性,与过量的重铬酸钠发生氧化还原反应生成二氧化碳、Cr3+和H2O,反应离子方程式为CH3OH+Cr2O72-+8H+→CO2↑+2Cr3++6H2O,可以防止环己酮继续被过量的重铬酸钠氧化,
故答案为:将过量的重铬酸钠还原,防止环己酮继续被氧化;CH3OH+Cr2O72-+8H+→CO2↑+2Cr3++6H2O;
(4)利用盐析原理,环己酮在氯化钠中的溶解度较小,有利于环己酮分层;乙醚提取液中含有少量的环己酮,所以将乙醚提取液和有机层合并的原因是减少环己酮在水中溶解造成的损失;
故答案为:降低环己酮的溶解度,有利于环己酮分层;减少环己酮在水中溶解造成的损失;
(5)由3 +1Na2Cr2O7+4H2SO4→3
+1Na2Cr2O7+4H2SO4→3 +1Na2SO4+1 Cr2(SO4)3+7H2O,则理论上生成环己酮的质量为:0.048mol×98g/mol=4.704g,所以所得产品的产率为$\frac{2.6}{4.704}$×100%=55.3%,
+1Na2SO4+1 Cr2(SO4)3+7H2O,则理论上生成环己酮的质量为:0.048mol×98g/mol=4.704g,所以所得产品的产率为$\frac{2.6}{4.704}$×100%=55.3%,
故答案为:55.3%.
点评 本题考查了环己酮的制备实验方案设计,涉及化学仪器、装置分析评价、物质的分离提纯、氧化还原反应配平、对数据的分析运用等,清楚制备的原理是解答的关键,题目难度中等.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:选择题
| A. | 向饱和AgCl水溶液中加入少量的NaCl固体,Ksp(AgCl)变大 | |
| B. | AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-) | |
| C. | 25℃时,当溶液中c(Ag+)×c(Cl-)=Ksp(AgCl)时,此溶液为AgCl的饱和溶液 | |
| D. | 将固体AgCl加入到浓KI溶液中,部分AgCl转化为AgI,故AgCl溶解度小于AgI |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知酸性高锰酸钾溶液是常用的强氧化剂,可以和草酸钠、二氧化硫等还原性物质发生氧化还原反应.
已知酸性高锰酸钾溶液是常用的强氧化剂,可以和草酸钠、二氧化硫等还原性物质发生氧化还原反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
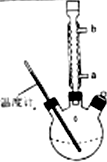
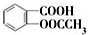 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐为主要原料合成阿司匹林,反应原理如下: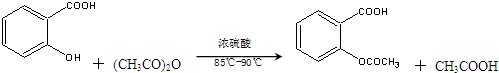
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水溶性 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 易水解 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
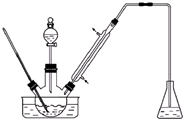 实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见图,相关物质的物理性质见附表).
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见图,相关物质的物理性质见附表).| 相对分 子质量 | 密度 /(g•cm-3) | 沸点/℃ | |
| 溴 | 160 | 3.119 | 58.8 |
| 苯甲醛 | 106 | 1.04 | 179 |
| 1,2-二氯乙烷 | 99 | 1.2351 | 83.5 |
| 间溴苯甲醛 | 185 | 1.587 | 229 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
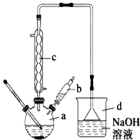 溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:
溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:| 苯 | 溴 | 溴苯 | |
| 密度/gcm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 在水中的溶解度 | 微溶 | 微溶 | 微溶 |
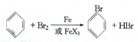 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸式滴定管未用待测溶液润洗 | |
| B. | 碱式滴定管未用待装溶液润洗 | |
| C. | 锥形瓶未用待装溶液润洗 | |
| D. | 在滴定前滴定管尖嘴部分有气泡,滴定后气泡消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2通入水中:Cl2+H2O=2H++Cl-+ClO- | |
| B. | 铜丝插入稀硝酸:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O | |
| C. | 向NaClO溶液中通入过量SO2:ClO-+SO2+H2O=HClO+HSO3- | |
| D. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com