
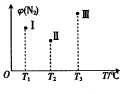
 �ֱ���Tl�桢T2�桢T3��ʱ��������500mL �ĺ����ܱ������о�����1molN2��2.5molH2��������Ӧ��N2��g��+3H2��g��?2NH3��g����H��0��ʵ���÷�Ӧtmin ʱN2�����������ͼ��ʾ������˵����ȷ���ǣ�������
�ֱ���Tl�桢T2�桢T3��ʱ��������500mL �ĺ����ܱ������о�����1molN2��2.5molH2��������Ӧ��N2��g��+3H2��g��?2NH3��g����H��0��ʵ���÷�Ӧtmin ʱN2�����������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ��t minʱ����͢�һ����ƽ��״̬ | |
| B�� | 2v��NH3��=3v��H2��ʱ��������������ƽ��״̬ | |
| C�� | ƽ����������л�������ƽ����Է���������С | |
| D�� | ��֪tminʱ������c��N2��=1mol/L����ʱ��Ӧƽ�ⳣ��K=0.5 |
���� A�����ڲ���ȷ������II�е����Ƿ�ﵽ��Сֵ����˲���ȷ��II�Ƿ�ﵽƽ��״̬��
B��û��ָ��H2��N2�����淴Ӧ���ʣ�
C���������غ㶨��֪�����������䣬�÷�ӦΪ�����С�ķ�Ӧ������N2�ĺ�����������ʵ������ƽ����Է���������С��
D������ƽ��ʱ�����ʵ����ʵ������ɼ���ƽ�ⳣ����
��� �⣺A�����ڲ���ȷ������II�е����Ƿ�ﵽ��Сֵ����˲���ȷ��II�Ƿ�ﵽƽ��״̬����δ��ƽ�⣬�¶�Խ�߷�Ӧ����Խ�죬��ͬʱ���ڵ����ĺ���Խ�ͣ�tminʱ�������ĺ�����Ȣ�ߣ��ʢ�ƽ�⣬��A����
B����Ϊһ����ʾ����Ӧ���ʡ���һ����ʾ�淴Ӧ���ʣ���Ӧ����ƽ�⣬��Ϊͬ�������ʣ�ѡ��A�й�ϵʽ���κ�����¶�����������˵������ƽ�⣬û��ָ��H2��N2�����淴Ӧ���ʣ�����˵����Ӧ�ﵽ��ƽ��״̬����B����
C���������غ㶨��֪�����������䣬�÷�ӦΪ�����С�ķ�Ӧ������N2�ĺ�����������ʵ�����ʢ�ƽ����Է���������С����C����
D.500mL �ĺ����ܱ������о�����1molN2��2.5molH2��������Ӧ��N2��g��+3H2��g��?2NH3��g����H��0��tminʱ������c��N2��=1mol/L����֪����0.5molN2��������1.5molH2������1molNH3��ƽ��ʱc��N2��=1mol/L��c��H2��=2mol/L��c��NH3��=2mol/L����K=$\frac{{2}^{2}}{1��{2}^{3}}$=0.5����D��ȷ��
��ѡD��
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ�߿��������ͺ�Ƶ���㣬��Ŀ�漰��ѧƽ����ƶ���ƽ�ⳣ���ļ����Ũ���صĹ�ϵ�����ڿ��鿼����ͼ��ķ��������Լ��Ի�ѧƽ������⣬�ѶȽϴ�


 �ظ���ʦ�㲦ϵ�д�
�ظ���ʦ�㲦ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ���ȣ�pH���� | |
| B�� | �����£���ˮ�м�����������KOH��c��OH-����� | |
| C�� | ��ˮ�е���ϡ���ᣬc��H+������ | |
| D�� | ��ˮ�м�����������NaClO��ƽ�������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Si��SiO2�ڳ����¶�����NaOH��Һ��Ӧ | |
| B�� | C��SiO2֮����Է�Ӧ�Ʊ�Si��ͬʱ�õ�CO | |
| C�� | Si��SiO2������������ᷴӦ | |
| D�� | Si��SiO2��H2SiO3����ͨ��һ����Ӧʵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʯ�뻥Ϊʯīͬ���칹�� | |
| B�� | ʯī�Ƚ��ʯ�ȶ� | |
| C�� | Ũ������ϡ����������Һ��Ӧ���к���Ϊ-57.3kJ | |
| D�� | ϡ�����ϡBa��OH��2��Һ��Ӧ����1molH2Oʱ����ЧӦ��-57.3kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 283.0kJ/mol | B�� | -566.0kJ/mol | C�� | 283.0kJ | D�� | 566.0kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
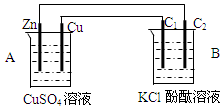 ��ͼװ�ý���ʵ�飬���ش���������
��ͼװ�ý���ʵ�飬���ش����������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
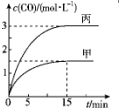 һ�������´��ڷ�ӦC��s��+H2O��g��?CO��g��+H2��g����H��0����ס����������������м���һ����C��H2O��g�������Һ��������м���һ����CO��H2�����������¶ȡ���Ӧ�����ʼ��������ס�����Ӧ������CO�����ʵ���Ũ����ʱ��仯��ͼ��
һ�������´��ڷ�ӦC��s��+H2O��g��?CO��g��+H2��g����H��0����ס����������������м���һ����C��H2O��g�������Һ��������м���һ����CO��H2�����������¶ȡ���Ӧ�����ʼ��������ס�����Ӧ������CO�����ʵ���Ũ����ʱ��仯��ͼ��| ���� | �� | �� | �� |
| �ݻ� | 0.5L | 0.5L | V |
| �¶� | T1�� | T2�� | T1�� |
| ��ʼ�� | 2mol C�� 1mol H2O��g�� | 1mol CO�� 1mol H2 | 4mol C�� 2mol H2O��g�� |
| A�� | ���������ݻ�V��0.5L | |
| B�� | �������У���Ӧ��ǰ15 min�ڵ�ƽ����Ӧ����v��H2��=0.15 mol•L-1•min-1 | |
| C�� | ���¶�ΪT1��ʱ����Ӧ��ƽ�ⳣ��K=2.25 | |
| D�� | �������У���ƽ��ʱn��H2O��=0.3 mol����T1��T2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com