
分析 (1)电解氢氧化钡溶液,在阳极上氢氧根离子失电子,在阴极上是氢离子得电子,据此回答;
(2)电解碳酸钠溶液,在阳极上氢氧根离子失电子,在阴极上是氢离子得电子,据此回答;
(3)电解氢氧化钠溶液,阴极发生还原反应生成氢气;电解NaCl溶液可得到氯气、氢气和氢氧化钠;
(4)用惰性电极电解硝酸银溶液时,阳极上氢氧根离子放电,阴极上银离子放电生成银.
解答 解:(1)电解氢氧化钡溶液,在阳极上氢氧根离子失电子4OH--4e-═O2+2H2O;在阴极上是氢离子得电子2H++2e-═H2↑,实质是电解水,总方程式为:$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,故答案为:阳极:4OH--4e-═O2+2H2O;阴极:2H++2e-═H2↑,总:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(2)电解碳酸钠溶液,在阳极上氢氧根离子失电子4OH--4e-═O2+2H2O;在阴极上是氢离子得电子2H++2e-═H2↑,实质是电解水,总方程式为:$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,故答案为:阳极:4OH--4e-═O2+2H2O;阴极:2H++2e-═H2↑,总:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(3)电解NaCl溶液可得到氯气、氢气和氢氧化钠,阴极发生还原反应生成氢气:2H++2e-═H2↑,阳极上是2Cl--2e-═Cl2↑,电解总方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,故答案为:阴极:2H++2e-═H2↑,阳极:2Cl--2e-═Cl2↑,总:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
(4)用惰性电极电解硝酸银溶液时,阳极上氢氧根离子放电,阴极上银离子放电生成银,所以阴极、阳极、电池反应式分别为4Ag++4e-=4Ag、4OH--4e-═O2+2H2O、4Ag++2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2+4H+,
故答案为:阴极:4Ag++4e-=4Ag;阳极:4OH--4e-═O2↑+2H2O;总:4AgNO3+2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4HNO3.
点评 本题以电解池为载体考查电极反应式的书写,为高频考点,明确离子放电书写是解本题关键,题目难度不大.


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,8gO2含有4nA个电子 | |
| B. | 标准状况下22.4 L的NH3溶于水,所得溶液中有nA个NH4+ | |
| C. | 200mL的5mol•L-1盐酸中含有nA个HCl分子 | |
| D. | 1mol Na被完全氧化生成Na2O2,失去2nA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去CO2 中少量CO,通过灼热氧化铜 | |
| B. | 除去NO中少量NO2,气体通入足量水中后,用浓硫酸干燥 | |
| C. | 除去KCl固体中少量K2CO3,加入足量盐酸后,蒸发、结晶 | |
| D. | 除去CuSO4 溶液中Fe2(SO4)3 杂质,加入足量铜粉,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
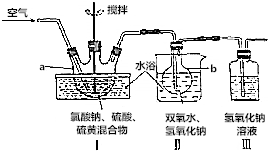
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 青石棉是一种硅酸盐材料 | |
| B. | 青石棉的化学组成可表示为Na2O•3FeO•Fe2O3•8SiO2•H2O | |
| C. | 1 mol青石棉中含有8 mol SiO2 | |
| D. | 1 mol青石棉能还原1 mol HNO3的稀硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
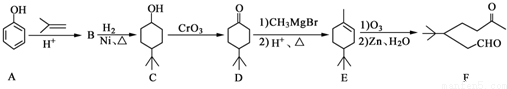
 .
. .同时满足下列条件的B的同分异构体(不包括B)共有11种:能与FeCl3溶液显紫色,苯环上只有两个取代基.
.同时满足下列条件的B的同分异构体(不包括B)共有11种:能与FeCl3溶液显紫色,苯环上只有两个取代基. (任写一种).
(任写一种).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCO3(s)═MgO(s)+CO2(g)△H=+1.366 kJ/mol | |
| B. | MgCO3(s)═MgO(s)+CO2(g)△H=-1.366 kJ/mol | |
| C. | MgCO3(s)═MgO(s)+CO2(g)△H=-114.7 kJ/mol | |
| D. | MgCO3(s)═MgO(s)+CO2(g)△H=+114.7 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3和盐酸 | B. | AlCl3和NaOH | C. | NaAlO2和硫酸 | D. | Na2CO3和BaCl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com