
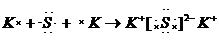 ,
,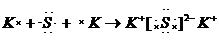 ;
;


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
| A、v(Fe)=0.05 mol/(L?min) |
| B、v(H2SO4)=0.1 mol/(L?min) |
| C、v(H2SO4)=0.5 mol/(L?min) |
| D、v(FeSO4)=0.1 mol/(L?min) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KMnO4 |
| B、Al2(SO4)3 |
| C、KClO3 |
| D、K2HPO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入的一元酸HA过量 |
| B、生成的盐RA不能发生水解 |
| C、加入的酸与碱的物质的量相等 |
| D、反应后溶液中C(A-)=C(R+) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 滴定次数 | 待测溶液 体积/mL | 草酸溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.50 | 23.70 |
| 2 | 25.00 | 1.02 | 26.03 |
| 3 | 25.00 | 0.00 | 24.99 |
- 4 |
2- 4 |
- 4 |
| 编号 | 温度/℃ | 酸化的H2C2O4溶液/mL | KMnO4溶液/mL | 溶液褪色时间/s |
| 1 | 25 | 5.0 | 2.0 | 40 |
| 2 | 25 | 5.0(另加少量可溶于水的MnSO4粉末) | 2.0 | 4 |
| 3 | 60 | 5.0 | 2.0 | 25 |
查看答案和解析>>
科目:高中化学 来源: 题型:

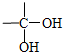
| 自动脱水 |
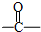
 ,反应④的化学方程式是
,反应④的化学方程式是查看答案和解析>>
科目:高中化学 来源: 题型:
 ,下列说法中正确的是( )
,下列说法中正确的是( )| A、D元素的负化合价为-2价时,E元素的最高化合价一定为+7 |
| B、B(OH)m为强碱时,A(OH)n也一定为强碱 |
| C、HnDOm为强酸时,E的非金属性一定很强 |
| D、HnCOm为强酸时,E的单质可能有强还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com