
| A. | 在空气中切开金属钠,光亮表面变暗:2Na+O2═Na2O2 | |
| B. | 向氯化铝溶液中加入过量氨水,产生白色沉淀:Al3++3OH-═Al(OH)3 | |
| C. | 将铁粉与水蒸气共热,产生气体:2Fe+3H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$ Fe2O3+3H2↑ | |
| D. | Al2O3 粉末溶于 NaOH 溶液中:Al2O3+2OH-═2AlO2-+H2O |
分析 A.不符合反应客观事实;
B.一水合氨为弱电解质,保留化学式;
C.不符合反应客观事实;
D.二者反应生成偏铝酸钠和水.
解答 解:A.在空气中切开金属钠,光亮表面变暗,是因为钠与氧气反应生成氧化钠,化学方程式:4Na+O2═2Na2O,故A错误;
B.向氯化铝溶液中加入过量氨水,产生白色沉淀,离子方程式:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故B错误;
C.将铁粉与水蒸气共热,反应生成四氧化三铁和氢气,化学方程式:3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$ Fe3O4+4H2,故C错误;
D.Al2O3 粉末溶于 NaOH 溶液中,离子方程式:Al2O3+2OH-═2AlO2-+H2O,故D正确;
故选:D.
点评 本题考查了化学方程式、离子方程式的书写,明确反应实质及反应条件对反应影响是解题关键,注意化学式拆分,注意反应遵循客观事实,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
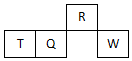 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中只有T为金属元素.下列判断错误的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中只有T为金属元素.下列判断错误的是( )| A. | 原子半径:T>Q | |
| B. | 元素非金属性:Q>R | |
| C. | 气态氢化物的热稳定性:R>Q | |
| D. | 最高价氧化物对应水化物的酸性:W>Q |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X为酸性氧化物,能与碱反应,不能与酸反应 | |
| B. | Y的化学式为SiH4 | |
| C. | X、Z都含有非极性共价键 | |
| D. | X与Mg在加热条件下反应的化学方程式为SiO2+2Mg$\frac{\underline{\;△\;}}{\;}$2MgO+Si |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溶解、过滤的方法提纯含有少量 BaSO4 的 BaCO3 | |
| B. | 用过滤的方法除去 NaCl 溶液中含有的少量淀粉胶体 | |
| C. | 用渗析的方法精制 Fe(OH)3 胶体 | |
| D. | 用分液的方法分离水和酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W和X形成的化合物可能含有非极性共价键 | |
| B. | X和Z形成的化合物常温下为固态 | |
| C. | W、X、Y、Z四种元素组成的化合物的水溶液可能呈酸性 | |
| D. | W、X、Y、Z四种元素两两之间均能形成二元化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com