
 HClO
HClO
 Mg
Mg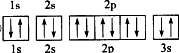 .
. 分析 (1)根据元素符号,判断元素原子的核外电子数,再根据核外电子排布规律来写;
(2)氮气分子中存在氮氮三键,氮原子最外层为8电子;HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键;
(3)先根据构造原理写出电子排布式,再画出价电子轨道排布图.
解答 解:(1)Cu元素为29号元素,原子核外有29个电子,所以核外电子排布式为:1s22s22p63s23p63d104s1;Cl元素为17号元素,原子核外有17个电子,所以核外电子排布式为:1s22s22p63s23p5;
故答案为:1s22s22p63s23p63d104s1;1s22s22p63s23p5;
(2)氮气分子中存在氮氮三键,氮原子最外层为8电子,N2的电子式为: ;HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键,次氯酸的电子式为:
;HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键,次氯酸的电子式为: ;
;
故答案为: ;
; ;
;
(3)C原子最外层4个电子,为2s22p2,两个电子分别占据2个p轨道,自旋反向相同,第一个电子层为1s2,
其电子轨道表达式为:
 ;
;
镁为12号元素,基态Mg原子正确的核外电子轨道表示式为: ;
;
故答案为:
 ;
; .
.
点评 本题考查了电子式、核外电子排布式、电子排布图等表示方法,题目难度中等,注意掌握常见的化学用语的概念及正确的表示方法,明确核外电子排布式的表示方法,侧重于考查学生对基础知识的应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 苯混有少量苯酚可加入溴水振荡后过滤除去 | |
| B. | 硝基苯和水可用分液漏斗分离 | |
| C. | 乙烷中混有少量乙烯可通入酸性高锰酸溶液再干燥除去 | |
| D. | 乙醇混有少量乙酸可通过蒸馏除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 我国自行研制的航母中使用到了大量特种钢,钢属于合金 | |
| B. | 珠三角是酸雨重灾区,酸雨主要成分是硝酸和碳酸 | |
| C. | 碘是人体必需微量元素,食盐加碘加的就是碘单质 | |
| D. | 节日里五颜六色的焰火利用的是金属单质的焰色反应,焰色反应属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池充电时,阴极发生还原反应生成Mo3S4 | |
| B. | 电池充电时,阳极反应为xMg-2xe-═xMg2+ | |
| C. | 电池放电时,Mg2+向负极迁移 | |
| D. | 电池放电时,正极反应为Mo3S4+2xe-+xMg2+═MgxMo3S4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯不能使酸性高锰酸钾溶液褪色,所以苯不能发生氧化反应 | |
| B. | 石油的主要成分是烃,石油经过分馏可制得汽油、乙烯等产品 | |
| C. | 丙烯分子中所有原子不可能在同一平面上 | |
| D. | 石油裂解的目的是为了提高轻质液体燃料的产量和质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体中一定含有乙烯 | B. | 混合气体中一定含有甲烷 | ||
| C. | 混合气体中一定含有丙烯 | D. | 混合气体中可能含有乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
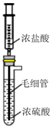 实验室用如图装置制备HCl气体.推压注射器活塞将浓盐酸慢慢注入到浓硫酸中,可制备少量干燥HCl气体,其原理分析不正确的是( )
实验室用如图装置制备HCl气体.推压注射器活塞将浓盐酸慢慢注入到浓硫酸中,可制备少量干燥HCl气体,其原理分析不正确的是( )| A. | 混合时放热使HCl溶解度减小 | |
| B. | 浓硫酸具有吸水性,吸收了盐酸中水分 | |
| C. | 浓盐酸具有挥发性,利于HCl气体逸出 | |
| D. | 浓盐酸中HCl以分子形式存在,利于HCl气体逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 H++B(OH)4-.
H++B(OH)4-.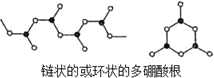 ,其组成可表示为(BO2)nn-.
,其组成可表示为(BO2)nn-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸可刻蚀石英制艺术品 | |
| B. | 活性炭、SO2和Na2O2都具有漂白作用,且漂白的化学原理相同 | |
| C. | 石油的裂化、煤的气化、Na2FeO4杀菌消毒均属于化学变化 | |
| D. | 氢氧化铁溶胶、水玻璃、淀粉溶液、PM2.5微粒均具有丁达尔效应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com