
【题目】常温下CH3COOH的电离常数为1.7×10-5,该温度下用0.1mol·L-1的醋酸溶液滴定10.00mL等物质的量浓度的碱ROH,滴定过程中加入醋酸的体积(V)与溶液中![]() 的关系如图所示。下列说法中正确的是
的关系如图所示。下列说法中正确的是
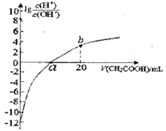
A. b点溶液显碱性
B. a>10.00
C. ROH的电离方程式为ROH![]() R++OH-
R++OH-
D. 25℃时,1mol·L-1的醋酸溶液中CH3COO-的浓度约为4.12×10-2mol·L-1(已知![]() =4.12)
=4.12)
【答案】B
【解析】试题分析:由图象可知,0.1mol·L-1的ROH的![]() = -12,c(OH-)=0.1mol/L,所以ROH是强碱。当加入0.1mol·L-1的醋酸溶液的体积为10.00mL时,两者恰好完全反应,得到呈碱性的CH3COOR溶液。A. b点加入20mL0.1mol·L-1的醋酸,醋酸过量,由图象可知,
= -12,c(OH-)=0.1mol/L,所以ROH是强碱。当加入0.1mol·L-1的醋酸溶液的体积为10.00mL时,两者恰好完全反应,得到呈碱性的CH3COOR溶液。A. b点加入20mL0.1mol·L-1的醋酸,醋酸过量,由图象可知,![]() >0,所以溶液显酸性,A不正确;B. a点
>0,所以溶液显酸性,A不正确;B. a点![]() =0,溶液呈中性,所以醋酸过量,a>10.00,B正确;C. ROH是强碱,其电离方程式为ROH=R++OH-,C不正确;D. 25℃时,1mol·L-1的醋酸溶液中CH3COO-的浓度约为
=0,溶液呈中性,所以醋酸过量,a>10.00,B正确;C. ROH是强碱,其电离方程式为ROH=R++OH-,C不正确;D. 25℃时,1mol·L-1的醋酸溶液中CH3COO-的浓度约为![]() 4.12×10-3mol·L-1,D不正确。本题选B。
4.12×10-3mol·L-1,D不正确。本题选B。


科目:高中化学 来源: 题型:
【题目】硫及硫化物广泛存在于自然界中,回答下列问题:
(1)基态S原子中,核外电子占据的最高能层的符号是___________,有__________种不同形状的电子云。
(2)(NH4)2SO4中O、N、S三种元素的第一电离能的大小关系为_______________________。
(3)中学化学常用KSCN检验Fe3+,列举一种与SCN-互为等电子体的分子:___________,SCN-中C原子的杂化方式为_________________。
(4)乙硫醇(CH3CH2SH)的相对分子质量比CH3CH2OH大,但乙醇的沸点高于乙硫醇的原因是_________________________________________________。
(5)PbS是一种重要的半导体材料,具有NaC1型结构(如图),其中阴离子采用面心立方最密堆积方式,X-射线衍射实验测得PbS的晶胞参数为a=0.594 n m。
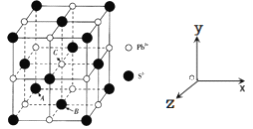
①已知坐标参数:A(0,0,0),B![]() ,则C的坐标参数为__________________。
,则C的坐标参数为__________________。
②PbS晶体中Pb2+的配位数为_________,r(S2-)为______nm。(已知![]() )
)
③PbS晶体的密度为_________g·cm-3。(列出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下发生反应:m A(g)+n B(g) ![]() p C(g)+q D(g) ΔH,反应物起始浓度相同,现在不同的温度T1和T2下反应分别达到平衡状态,B转化率与温度的关系如图所示,则下列叙述正确的是
p C(g)+q D(g) ΔH,反应物起始浓度相同,现在不同的温度T1和T2下反应分别达到平衡状态,B转化率与温度的关系如图所示,则下列叙述正确的是

A. 平衡时D的体积分数:状态Ⅱ大于状态Ⅰ B. T1>T2
C. 平衡时正反应速率:状态Ⅱ比状态Ⅰ大 D. ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学中有很多有趣的分子,比如图中所示分子被化学家命名为“小狗烯”,下列关于“小狗烯”的说法错误的是
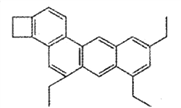
A. “小狗烯”的分子式是C26H26 B. “小狗烯”中含有四个苯环
C. “小狗烯”中所有碳原子一定共面 D. “小狗烯”可以发生加成反应、氧化反应和取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月5日,中国首架按照国际标准研制,拥有自主知识产权的大型客机C-919在上海浦东机场首飞,科学家在实验室研究利用催化技术将飞机尾气中的NO和CO转变成CO2和N2,其反应为2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH<0。
N2(g)+2CO2(g) ΔH<0。
(1)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是____________。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
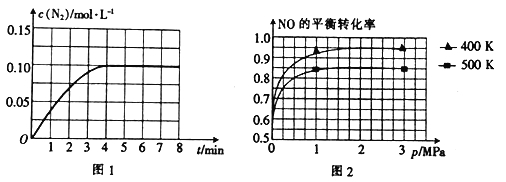
(2)若将1 molNO和2 mol CO通入2 L的恒容密闭容器中,在一定条件下发生上述反应,反应中生成的N2的物质的量浓度随时间的变化情况如图1所示。则NO从反应开始到平衡时的平均反应速率v(NO)=_________,4 min末CO的浓度为_____________ molL-1。
(3)已知上述反应中NO的平衡转化率与压强、温度的关系如图2所示。工业上催化装置比较适合的温度和压强是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取10mL10%的NaOH溶液,再加入约2 mL1%的硫酸铜溶液,得到强碱性的混合液。下列各对物质不能用这碱性混合物鉴别的是( )
A. 葡萄糖与蔗糖 B. 蛋白质与淀粉
C. 硬脂酸与油酸 D. 甲酸钠与乙酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2。

实验步骤如下:
①连接好实验装置,检查装置的气密性;
②把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为16.0g;
③加热,开始反应,直到不再有气体产生为止;
④测量排入量筒中水的体积为284.3mL,换算成标准状况下氧气的体积为279.0mL;
⑤准确称量试管和残留物的质量为15.6g。
根据上述实验过程,回答下列问题:
(1)如何检查装置的气密性?______.
(2)以下是测量收集到气体体积必须包括的几个步骤: ①调整量筒的高度使广口瓶和量筒内的液面高度相同;②使试管和广口瓶内气体都冷却至室温;③读取量筒内液体的体积,这三步操作的正确顺序是___________________________(请填写步骤代号),进行③的实验操作时,若仰视读数,则读取氧气的体积_______________(填“偏大”、“偏小”或“无影响”)。
(3)实验过程中产生氧气的物质的量是___________________mol;实验测得氧气的气体摩尔体积是____________L/mol(列出算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
以有机物A 合成聚酯类高分子化合物F 的路线如下:

已知: 
(1) A生成B 的反应类型为_________,C 中官能团的名称为__________ 。
(2) D 与NaOH 水溶液反应的化学方程式为__________ 。
(3) ①E 生成F 的化学方程式为__________。
②若F的平均相对分子质量为20000,则其平均聚合度为________ (填选项字母)。
A.54 B.108 C.119 D.133
(4) E 在一定条件下还可以合成含有六元环结构的G,G 的结构简式为__________。
(5) 满足下列条件的C 的同分异构体有___种(不考虑立体异构)。
①含有1个六元碳环,且环上相邻4 个碳原子上各连有一个取代基
②1mol 该物质与新制氢氧化铜悬浊液反应产生2mol 砖红色沉淀
(6) 写出以![]() 为原料(其他试剂任选) 制备化合物
为原料(其他试剂任选) 制备化合物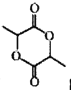 的合成路线,请用以下方式表示:
的合成路线,请用以下方式表示: 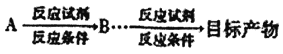 。___________________。
。___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com