
| A. | 2NaCl(熔融)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑ | B. | MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑ | ||
| C. | 3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe | D. | Cu+2FeCl3═CuCl2+2FeCl2 |
分析 金属冶炼是工业上将金属从含有金属元素的矿石中还原出来的生产过程.金属的活动性不同,可以采用不同的冶炼方法.
金属冶炼的方法主要有:
热分解法:对于不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来(Hg及后边金属);
热还原法:在金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来(Zn~Cu);
电解法:活泼金属较难用还原剂还原,通常采用电解熔融的金属化合物的方法冶炼活泼金属(K~Al).
解答 解:A.钠性质活泼,用电解熔融氯化钠方法制取,故A正确;
B.镁性质活泼,用电解熔融氯化镁方法制取,故B正确;
C.铁熔点高,活泼性弱于铝,可用铝热反应制取,故C正确;
D.铜与氯化铁反应得不到金属,故D错误;
故选:D.
点评 本题考查了冶炼金属的一般方法和原理,明确物质的性质是解题关键,注意活泼性不同的金属冶炼的方法不同,本题难度不大.


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
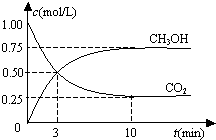 恒温恒容密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应:
恒温恒容密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应:| A. | 该密闭容器的体积为1 L | |
| B. | 反应达平衡,氢气的转化率为0.75 | |
| C. | 反应达平衡,氢气平均反应速率0.075 mol/(L•min) | |
| D. | CO2或H2O物质的量不再改变时反应达平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 探究SO2的性质.甲组同学将SO2分别通入下列3种溶液中.
探究SO2的性质.甲组同学将SO2分别通入下列3种溶液中.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自发进行的化学反应不一定是放热反应 | |
| B. | 自发过程将导致体系的熵增大 | |
| C. | △H-T△S<0的反应,不需要任何条件就可自发进行 | |
| D. | 同一物质的气、液、固三种状态的熵值依次增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | N≡N | N-H |
| 键能(kJ/mol) | 436 | 946 | 391 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO4•10H2O脱水是吸热过程 | |
| B. | 较长时间制冷是由于Na2SO4•10H2O脱水是较慢的过程 | |
| C. | 铵盐在该条件下,发生的复分解反应是吸热反应 | |
| D. | NH4NO3溶于水会吸收热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g)△H<0,如图表示该反应的速率随时间变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )
某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g)△H<0,如图表示该反应的速率随时间变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )| A. | t2时升高了温度 | |
| B. | t3时降低了温度 | |
| C. | t5时增大了压强(缩小容器体积) | |
| D. | 平衡状态时,t6时刻Z的百分含量最低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(OH-)=10-13mol•L-1的溶液中:Na+、NH4+、Cl-、NO3- | |
| B. | 1.0 mol•L-1KI溶液中:Mg2+、Fe2+、SO42-、ClO- | |
| C. | c(Fe3+)=0.1 mol•L-1的溶液中:Na+、NH4+、HCO3-、I- | |
| D. | 饱和氨水中:NH4+、Ag+、SO42-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com