
【题目】营养强化剂是为了食物的营养价值而强制添加的物质,比如食盐中加碘,是为了预防碘缺乏病的发生。食盐中加碘,所加“碘”指的是( )
A.碘单质B.碘酸钾
C.碘化钾D.次碘酸钾
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】人们的饮食追求是“吃得营养,吃出健康”,下列相关说法不正确的是( )
A.每天都应摄入一定量的蛋白质
B.油脂会使人发胖,故禁食油脂
C.过多摄入微量元素不利于健康
D.每天食用少量纤维素有利于健康
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲图是部分短周期元素的常见化合价与原子序数的关系图:
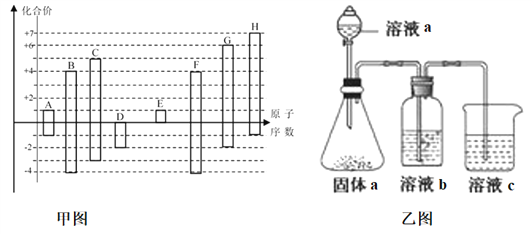
请回答下列问题:
(1)D元素在周期表中的位置为___________,D和G的简单氢化物中沸点高的是___________ (写化学式),A和E形成的化合物的电子式为_____________。
(2)D、E、G、H的简单离子半径由大到小的顺序为__________________________。(用化学式表示)
(3)二元化合物X是含有C元素的18电子分子,1molX(l)在25℃ 101kPa下完全燃烧放出622kJ的热量,写出表示X燃烧热的热化学方程式________________________________。
(4)H的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是H的单质,且当有28mol电子转移时,常温共产生9mol气体,写出该反应的化学方程式___________________________________。
(5)由上述元素中的几种组成a、b、c各物质,某同学设计实验用乙图装置证明元素B、C、F的非金属性强弱(其中溶液b和溶液c均为足量)。
①溶液a和b分别为________,________(填化学式)。
②溶液c中的离子方程式为__________________________________________。
③请从原子结构的角度解释非金属性C>B的原因 ____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。为此,他们设计了如下装置验证所产生的气体成分。
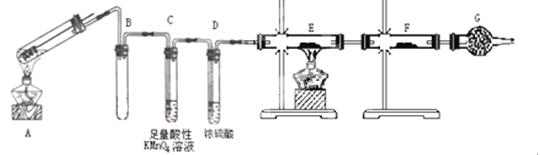
(1)填写装置的作用:B___________,C___________,G___________。
(2)证明有S02生成的实验现象是_____________________。
(3)可以证明所产生的气体中含有H2的实验现象是:E中:___________,F中:_________。如果去掉装置D,还能否根据F中的现象判断气体中有H2?_________(填能”或“不能”),原因是_________________________。
(4)反应后A的溶液中含有Fe3+和Fe2+,检验其中Fe2+的方法是____________。
(5)若将铁丝换成铜丝,反应后的溶液没有出现预计的蓝色溶液,而出现了大量白色固体。原因是___________________________;要确认有CuSO4生成,待试管冷却后,____________。写出铜与浓硫酸反应的离子方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素可以形成多种化合物。回答以下问题:
(1)基态氮原子的价电子排布式是_________________。
(2)C、N、O三种元素第一电离能从大到小的顺序是____________。
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子的空间构型是_______________;N2H4分子中氮原子轨道的杂化类型是___________。
②肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)===3N2(g)+4H2O(g) △H=-1038.7kJ·mol-1,若该反应中有4mol N-H键断裂,则形成的π键有________mol。
③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在__________(填标号)
a. 离子键 b. 共价键 c. 配位键 d. 范德华力
(4)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。

下列分子或离子中,能被该有机化合物识别的是_________(填标号)。
a. CF4 b. CH4 c. NH4+ d. H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列正确的是( )
A.碳酸的电离:H2CO3?H++HCO ![]()
B.硫化钠水解:S2﹣+2H2O?H2S↑+2OH﹣
C.Na2CO3溶液中:c(HCO ![]() )>c(OH﹣)
)>c(OH﹣)
D.NH4Cl溶液中,c(NH ![]() )>c(Cl﹣)
)>c(Cl﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】弱酸H2A溶液中存在H2A、HA-和A2- 三种形态的粒子,其物质的量分数 δ( X)=  随溶液pH变化的关系如图所示,下列说法正确的是( )
随溶液pH变化的关系如图所示,下列说法正确的是( )

A. 曲线①代表的粒子是HA-
B. 0.1mol·L -1的NaHA溶液中存在:c(Na+ )+c(A2- )+c(H2A)+c(HA- )>0.2 mol·L-1
C. 若图中的a值为4.2,则H2A的第二步电离平衡常数Ka1为10-4.2
D. 随着PH的升高,  的比值先增大后减小
的比值先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg ![]() 的变化如图所示,下列叙述错误的是( )
的变化如图所示,下列叙述错误的是( ) 
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH﹣)相等
D.当lg ![]() =2时,若两溶液同时升高温度,则
=2时,若两溶液同时升高温度,则 ![]() 增大
增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com