
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| C(NH3)/mol•L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
分析 恒温下,往一个2L的密闭容器中充入2.6mol H2和1mol N2,20min处于平衡状态,平衡时NH3浓度为0.2mol/L,则:
N2(g)+3H2(g)?2NH3(g)
起始量(mol/L):0.5 1.3 0
变化量(mol/L):0.1 0.3 0.2
平衡量(mol/L):0.4 1 0.2
平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$,以此解答该题.
解答 解:恒温下,往一个2L的密闭容器中充入2.6mol H2和1mol N2,20min处于平衡状态,平衡时NH3浓度为0.2mol/L,则:
N2(g)+3H2(g)?2NH3(g)
起始量(mol/L):0.5 1.3 0
变化量(mol/L):0.1 0.3 0.2
平衡量(mol/L):0.4 1 0.2
则反应达到化学平衡时,氮气的浓度为0.4 mol/L,
平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$=$\frac{0.{2}^{2}}{0.4×{1}^{3}}$=0.1.
故答案为:0.4 mol/L;0.1.
点评 本题考查化学平衡计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握计算的思路,掌握平衡常数的计算,需要学生具备扎实的基础,难度中等.


科目:高中化学 来源: 题型:实验题

| 优等品 | 一等品 | 合格品 | |
| 外观 | 白色结晶,无可见机械杂质 | 无可见机械杂质 | |
| 氮(N)含量 | ≥21.0% | ≥21.0% | ≥20.5% |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 做好空气质量预报工作,以便空气污染时及时采取防护措施 | |
| B. | 推广“绿色自由”计划,吸收空气中的CO2并利用廉价能源合成汽油 | |
| C. | 将工业废水“再生”处理,用于道路保洁、城市喷泉和洗车等 | |
| D. | 利用风能、生物能发电,强制实施火力发电用煤的脱硫处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将煤液化、气化,有利于提高燃料的燃烧效率,减少污染物的排放 | |
| B. | 侯氏制碱法,向饱和NaCl溶液中先通入CO2再通入氨气制取纯碱 | |
| C. | 电解精炼铜时,同一时间内阳极溶解铜的质量与阴极析出铜的质量相等 | |
| D. | 工业生产硫酸时,建立高烟囱可以降低地面SO2的浓度,减少空气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
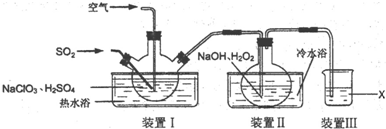
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不变 | B. | 增大 | C. | 减小 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10℃时0.1 mol/L Na2S2O3和0.1 mol/L H2SO4各 5 mL | |
| B. | 20℃时0.1 mol/L Na2S2O3和0.1 mol/L H2SO4各 5 mL | |
| C. | 10℃时0.1 mol/L Na2S2O3和0.1 mol/L H2SO4各5 mL,加水10mL | |
| D. | 20℃时0.2mol/L Na2S2O3和0.1 mol/LH2SO4各5 mL,加水10 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 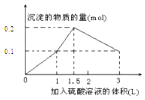 | B. | 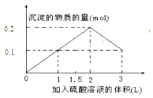 | ||
| C. | 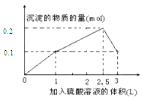 | D. | 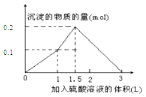 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com