
【题目】对于A+2B(g)![]() nC(g)。在一定条件下达到平衡后,改变下列条件,请回答:
nC(g)。在一定条件下达到平衡后,改变下列条件,请回答:
(1)当n=3时,增压,平衡不移动,则A为______态。
(2)若A为固态,增大压强,C的组分含量增加,则n_________,反应的平衡常数__________(填增大、减小或不变)。
(3)升温,平衡向右移动,达到新平衡前,υ正 ______υ逆(填>、< 或 =),则该反应的逆反应为_______热反应,反应的平衡常数__________(填增大、减小或不变)。
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 丁达尔效应不是胶体特有的现象,溶液和浊液也有
B. 胶体与其它分散系的本质区别是胶体有丁达尔效应,而其它分散系却没有
C. 胶体粒子的直径小于1nm
D. 丁达尔效应可用于鉴别胶体和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72 L,若反应过程中溶液的体积保持不变,则下列说法正确的是( )
A.标准状况下,反应过程中得到7.84 L的气体
B.最终得到的溶液中c(Na+)=c(Cl﹣)+c(OH﹣)
C.最终得到7.8 g的沉淀
D.最终得到的溶液中c(Na+)=1.5 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaCl固体配制0.1 mol·L-1的NaCl溶液,下列操作或说法正确的是
A.将5.85gNaCl固体溶于1 L水中可配成0.1 mol·L-1的NaCl溶液
B.称量时,将固体NaCl直接放在天平左盘上
C.固体溶解后,将溶液转移到容量瓶中,然后向容量瓶中直接加水稀释到刻度线
D.配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①②③④四种金属片两两相连浸入稀硫酸中都可组成电池,①②相连时,电路电流从②流向①;①③相连时,③为正极,②④相连时,②有气泡逸出现,③④相连时,③的质量减少,据此判断这四种金属活动性由大到小的顺序是
A. ①③②④ B. ①③④② C. ③④②① D. ③①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是生命的摇篮,有关海洋中部分资源的利用如图所示,回答下列问题 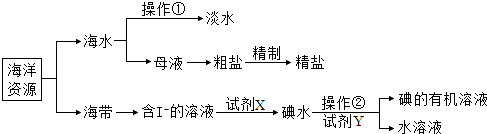
(1)操作①是 , 操作②使用的主要玻璃仪器是;
(2)含I﹣溶液中加入试剂X的目的是将I﹣(填“氧化”或“还原”)成I2;试剂Y选择原则包括:与碘不反应、碘在Y中的溶解度大于在水中的溶解度和;
(3)为除去粗盐中含有硫酸钠、氯化镁、氯化钙等杂质,应加入过量的氯化钡、氢氧化钠、碳酸钠等物质,将杂质转化为沉淀过滤除去,再向滤液中加入适量盐酸得到精盐水.该工程示意如下: 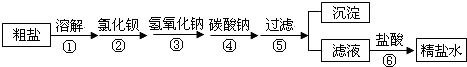
以下叙述正确的是(双选)
A.①操作中需要进行搅拌,目的是提高氯化钠的溶解度
B.③、④两步操作顺序可以颠倒
C.⑤操作得的沉淀中共有三种物质
D.⑥操作中,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH调为7
(4)海水资源也可以提炼出铝,铝制品与铁制品相比,在空气中不易锈蚀,原因是:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由 NaHS、MgSO4、NaHSO3 组成的混合物中,已知硫元素的质量分数w(S)=a%,则氧元素的质量分数w(O)为( )
A.1.75a%
B.1.25a%
C.1﹣1.75a%
D.1﹣1.25a%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重水(D2O)是重要的核工业原料,下列说法错误的是
A. 氘(D)的原子核外有1个电子 B. 1 H与D互称同位素
C. H2O与D2O互称同素异形体 D. 1 H218O与D216O的相对分子质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,由加成反应引起的是
A. 乙烯通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色
B. 含碳原子较多的烷烃加热、加压、催化剂条件下反应生成含碳原子较少的烷烃和烯烃
C. 在光照条件下,C2H6与Cl2反应生成了油状液体
D. 在催化剂作用下, 乙烯与水反应生成乙醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com