
| A. | ①②③ | B. | ⑤ | C. | ④ | D. | ①②③④ |
分析 由2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O、2Na2O2+2H2O=4NaOH+O2、2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2、2Na2O2+2CO2=2Na2CO3+O2,可知过氧化钠增加的质量即为H2、CO的质量,因此只要是CO或H2或它们的混合气体或化学组成符合(CO)m•(H2)n时m=n,若n>m,则不符合(CO)m•(H2)n,以此来解答.
解答 解:由上述分析可知,n>m,则不符合(CO)m•(H2)n,
①②③均符合(CO)m•(H2)n,④HCOOCH3化学式改写为(CO)2•(H2)2符合(CO)m•(H2)n;
⑤CH3CHO化学式改写为(CO)2•(H2)2.C,燃烧后与足量的过氧化钠完全反应,过氧化钠增质量加了n g,且n>m,
故选B.
点评 本题考查化学反应方程式的计算,为高频考点,把握过氧化钠增重的实质、化学式的变形为解答的关键,侧重分析与计算能力的考查,注意过氧化钠的性质,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2CH2CH2Cl | B. | 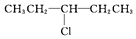 | ||
| C. | 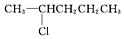 | D. | 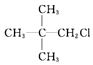 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 五种元素中有两种金属元素 | |
| B. | 元素C、D、E的最高价氧化物对应水化物的酸性增强 | |
| C. | 元素D、E分别与元素A形成化合物的稳定性:A2D>AE | |
| D. | 元素B、D、E的简单离子半径大小为:B>D>E |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用图所示装置进行下列各组实验,具体操作如下:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图所示装置进行下列各组实验,具体操作如下:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选项 | ①中物质 | ②中物质 | 预测的实验现象 |
| A | 浓盐酸 | 二氧化锰固体 | 立即产生气泡 |
| B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C | 氯化铝溶液 | 浓氢氧化钠溶液 | 立即产生白色沉淀 |
| D | 稀硫酸 | 滴有石蕊的亚硫酸钠溶液 | 溶液逐渐变红 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 日常生活中常见的聚乙烯、聚氯乙烯、聚四氟乙烯都可以通过加聚反应得到 | |
| B. | 等质量CH4和C4H8分别在氧气中完全燃烧,CH4的耗氧量小于C4H8 | |
| C. | 苯与溴水混合,反复振荡后溴水层褪色,这是由于发生了取代反应 | |
| D. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑥⑦ | B. | ①⑤ | C. | ③⑧ | D. | ③⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化硼液态时能导电而固态时不导电 | |
| B. | 氯化硼中心原子采用sp杂化 | |
| C. | 氯化硼分子与氯化铝分子互为等电子体,都是非极性分子 | |
| D. | 氯化硼的熔沸点与氯硼键的键能大小有关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com