
【题目】凤凰石是一种用于建材装饰的硅酸盐矿物,已知某地出产的凤凰石可看作由主要成分硅酸铜盐X·3H2O(摩尔质量=334g/mol)与含氧酸盐杂质Y共同组成,X、Y均含三种元素,工业上利用下列流程制备铜盐,在溶液Ⅱ中滴入KSCN溶液显血红色。

请回答:
(1)杂质Y中除氧以外还含有的元素为_____(填元素符号),x的化学式为_______。
(2)如果王溶液Ⅱ中继续加入H2O2,发现有气泡产生,有观点认为是Y中的某元素离子将H2O2氧化所导致,写出反应的离子方程式__________。
【答案】 Fe、C Cu2SiO6或2CuO·2SiO2 2Fe3++H2O2=2Fe2++2H++O2↑
【解析】试题分析:在溶液Ⅱ中滴入KSCN溶液显血红色,说明含有Fe3+;X、Y的混合物加入足量盐酸,生成二氧化碳,Y中除氧以外还含有的元素为Fe、C;X中含有Cu、Si、O元素,根据相对分子质量计算化学式;(2)Y中具有氧化性的只可能是Fe3+;
解析:(1)溶液Ⅱ中含有Fe3+;X是硅酸铜盐,X、Y的混合物加入足量盐酸,放出生成二氧化碳,所以Y中除氧以外还含有的元素为Fe、C,生成氯化铜的物质的量27g÷135 g/mol=0.2 mol;二氧化硅的物质的量12 g÷60 g/mol=0.2 mol,即 n(Cu):n(Si)=1:1,则x的化学式可表示为(CuO·SiO2)n,X·3H2O的摩尔质量334g/mol,X的摩尔质量280g/mol,n= 280÷140=2,x的化学式为2CuO·2SiO2;(2)Y中的Fe3+将H2O2氧化为氧气的离子方程式2Fe3++H2O2=2Fe2++2H++O2↑。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列关于乙烯的叙述不正确的是( )
A.乙烯的化学性质比乙烷活泼
B.乙烯燃烧时火焰明亮,同时有少量黑烟
C.乙烯可作香蕉等水果的催熟剂
D.乙烯双键中的一个键可以断裂,容易发生加成反应和取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.50%的ZnS和12.8%的CuS及少量的Fe3O4。某同学用15.0 g该废催化剂为原料,回收锌和铜。采用的实验方案如下,回答下列问题:
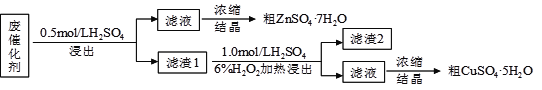
已知:ZnS与稀硫酸反应,且化合价不变; CuS既不溶解于稀硫酸,也不与稀硫酸反应
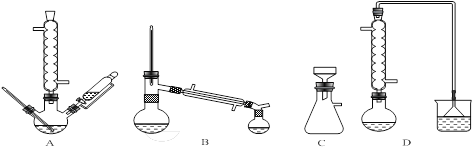
(1)在下列装置中,第一次浸出反应装置最合理的___________(填标号)。
(2)滤液1中含有Fe2+,选用提供的试剂进行检验,检验方法如下: 。
(提供的试剂:稀盐酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水)
(3)本实验要用到抽滤,设所用的洗涤剂为X,抽滤洗涤沉淀的操作 。
(4)写出第二次浸出的化学反应方程式 ,向盛有滤渣1的反应器中加H2SO4和H2O2溶液,应先加 。
(5)滤渣2的主要成分是 。浓缩、结晶得到硫酸锌晶体的主要仪器名称是 。
(6)某同学在实验完成之后,得到1.50 g CuSO4·5H2O,则铜的回收率为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期。A是原子半径最小的元素;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍;E有“生物金属”之称,E4+和氩原子的核外电子排布相同。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1 : 1的化合物N是常见的有机溶剂。
请回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)A2D2分子的电子式为____________,属于___________分子(填“极性”或“非极性”),E的基态原子的外围电子排布式为____________。
(2)B、C、D三种元素的第一电离能由小到大的顺序为____________。
(3)C元素形成含氧酸酸性强弱:HNO3____________HNO2(填“>”或“<”)NO3—的空间构型是___________,NO2—中心原子的杂化方式为___________
(4)下列叙述正确的是____________(填序号)。
A. M是极性分子,N是非极性分子
B. M和BD2分子中的中心原子均采用sp2杂化
C. N分子中含有6个σ键和1个大π键
D. BD2晶体的熔点、沸点都比二氧化硅晶体的低
(5)已知:①E的一种氧化物Q,其晶胞结构如图所示:

①Q(s)+2Cl2(g)=ECl4(l)+D2(g) △H=+140kJ/mol
②2B(s)+D2(g)=2BD(g) △H=-221kJ/mol
写出物质Q和焦炭、氯气反应生成液态ECl4和BD气体的热化学方程式:____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同一温度下,强电解质溶液a、弱电解质溶液b、金属导体c三者的导电能力相同,若升高温度后,它们的导电能力强弱顺序是( )
A. b>a>c B. a=b=c
C. c>a>b D. b>c>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是 ( )
A. 1 L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1 mol/L
B. 从1L2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L
C. 配制500mL0.1 mol·L-1的CuSO4溶液,需8.0g 无水CuSO4
D. 中和100mL1mol/L的H2SO4溶液,需NaOH为4.0 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg﹣AgCl 电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:2AgCl+Mg═Mg2++2Ag+2Cl﹣ . 有关该电池的说法正确的是( )
A.Mg 为电池的正极
B.负极反应为 AgCl+e﹣=Ag+Cl﹣
C.可用于海上应急照明供电
D.电池工作时,电解质溶液质量不断减轻
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com