
【题目】有机物C常用于食品行业。已知9.0gC在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,其质谱图如图所示,则:
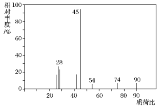
(1)C的分子式是___。
(2)若C能与NaHCO3溶液发生反应,则C中一定含有的官能团名称是_____。又知C分子的核磁共振氢谱有4个峰,峰面积之比是1∶1∶1∶3,则C的结构简式是_____。写出C与NaHCO3溶液反应的化学方程式__。
(3)0.1molC与足量Na反应,在标准状况下产生H2的体积是_____L。
【答案】C3H6O3 羧基 CH3CH(OH)COOH CH3CH(OH)COOH+NaHCO3→CH3CH(OH)COONa+CO2↑+H2O 2.24
【解析】
由图中最大质荷比可确定相对分子质量为90,5.4g水的物质的量为![]() ,n(H)=0.6 mol,13.2g二氧化碳的物质的量为
,n(H)=0.6 mol,13.2g二氧化碳的物质的量为![]() ,n(C)=n(CO2)=0.3 mol,此有机物9.0g含O元素质量为9.0g-0.6g-0.3×12 g=4.8 g,n(O)=
,n(C)=n(CO2)=0.3 mol,此有机物9.0g含O元素质量为9.0g-0.6g-0.3×12 g=4.8 g,n(O)=![]() ,故n(C):n(H):n(O)=0.3mol:0.6mol:0.3mol=1:2:1,即实验式为CH2O,设分子式为(CH2O)n,A的相对分子质量为90,可得30n=90,解得:n=3,故有机物A为C3H6O3。
,故n(C):n(H):n(O)=0.3mol:0.6mol:0.3mol=1:2:1,即实验式为CH2O,设分子式为(CH2O)n,A的相对分子质量为90,可得30n=90,解得:n=3,故有机物A为C3H6O3。
(1)由上述分析可知,其相对分子质量是90,则C的分子式是C3H6O3;
(2)C能与NaHCO3溶液发生反应,C一定含有羧基;核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则分子中4种H原子的数目为1、1、1、3,分子中含有1个COOH,和1个-CH3,则A的结构简式为CH3CH(OH)COOH,其与NaHCO3溶液反应的化学方程式为CH3CH(OH)COOH+NaHCO3→CH3CH(OH)COONa+CO2↑+H2O;
(3)C中的羟基和羧基均能与Na反应,1molC提供2molH,生成1molH2,则0.1molC与钠反应,生成H2在标准状况下的体积为2.24L。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】玫瑰的香味物质中包含蚽烯,蚽烯的键线式为:![]() 。
。
(1)1 mol蚽烯最多可以跟____ mol H2发生反应。
(2)写出蚽烯跟等物质的量的Br2发生加成反应所得产物的可能的结构_______________ (用键线式表示)。
(3)有机物A是蚽烯的同分异构体,分子中含有“![]() ”结构,A可能的结构为______(用键线式表示)。
”结构,A可能的结构为______(用键线式表示)。
(4)写出![]() 与Cl2发生1,4-加成反应的化学方程式____________。
与Cl2发生1,4-加成反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.分子式为CH4O和C2H6O的物质一定互为同系物
B.甲烷、乙烯和苯在工业上都可通过石油分馏得到
C.苯酚钠溶液中通入少量二氧化碳生成苯酚和碳酸钠
D.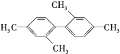 分子中至少有11个碳原子处于同一平面上
分子中至少有11个碳原子处于同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组研究含一定浓度Fe2+的溶液在不同条件下被氧气氧化的氧化率,实验结果如图所示,判断下列说法不正确的是
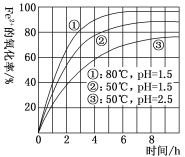
A.温度越高氧化率越大
B.pH越小氧化率越大
C.Fe2+的氧化率仅与溶液的pH和温度有关
D.实验说明降低pH、升高温度有利于提高Fe2+的氧化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A的相对分子质量为84。回答下列问题:
(1)烃A的分子式为__。下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不变的是_____;若总质量一定,充分燃烧消耗氧气的量不变的是_____。
A.C7H8 B.C6H14 C.C7H14 D.C8H8
(2)若烃A分子中所有的碳原子在同一平面上,且该分子的一氯取代物只有一种。则A的结构简式为__。若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g) +O2(g)=2H2O(g) ΔH =-483.6 kJmol1
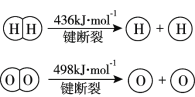
下列说法不正确的是
A.该反应可作为氢氧燃料电池的反应原理
B.破坏1 mol H-O键需要的能量是463.4 kJ
C.H2的燃烧热ΔH<-241.8 kJ·mol1
D.H2(g)中的H-H键比H2O(g)中的H-O键牢固
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T1时,向容积为2 L 的密闭容器甲、乙中分别充入一定量的CO(g)和H2O(g),发生反应:CO(g) + H2O(g) ![]() CO2(g) + H2(g) H = -41 kJ/mol。数据如下,下列说法不正确的是
CO2(g) + H2(g) H = -41 kJ/mol。数据如下,下列说法不正确的是
容器 | 甲 | 乙 | ||
反应物 | CO | H2O | CO | H2O |
起始时物质的量(mol) | 1.2 | 0.6 | 2.4 | 1.2 |
平衡时物质的量(mol) | 0.8 | 0.2 | a | b |
A. 甲容器中,平衡时,反应放出的热量为16.4 kJ
B. T1时,反应的平衡常数K甲 = 1
C. 平衡时,乙中CO的浓度是甲中的2倍
D. 乙容器中,平衡时CO的转化率约为75%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】染料化工企业产生的废水中含有高浓度的氨氮(氨和铵盐)成分,直接排放会造成环境污染。实验小组探索下列方法对氨氮废水进行处理。

(1)实验室检测上述废水中是否含有氨氮的方法是___。
(2)“吹脱”步骤中,在废水池的底部吹入大量热气泡,其目的是___。
(3)“氧化”步骤中加入了微生物,NH3被氧化为N2。反应的化学方程式为___。
(4)“沉淀"步骤中将剩余的NH3·H2O转化为NH4MgPO46H2O沉淀,发生反应的离子方程式为___。NH4MgPO46H2O在农业生产中具有重要应用价值,其原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用一氧化碳合成可再生能源甲醇。
(1)已知:Ⅰ.3CO(g)+6H2(g)![]() CH3CH=CH2(g)+3H2O(g) △H1=-301.3kJ/mol;
CH3CH=CH2(g)+3H2O(g) △H1=-301.3kJ/mol;
Ⅱ.3CH3OH(g)![]() CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol。
CH3CH=CH2(g)+3H2O(g) △H2=-31.0kJ/mol。
则CO与H2合成气态甲醇的热化学方程式为___________________________________
(2)某科研小组在Cu2O/ZnO作催化剂的条件下,在500℃时,研究了n(H2):n(CO)分别为2:1、5:2时CO的转化率变化情况(如图1所示),则图中表示n(H2):n(CO)=2:1的变化曲线为___________(填“曲线a”或“曲线b”),原因是_______________________________。
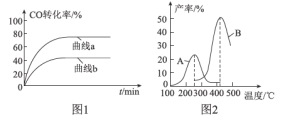
(3)某科研小组向密闭容器中充入一定量的CO和H2合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得CH3OH的产率与温度的关系如图2所示。下列说法正确的是____________(填选项字母)。
a.使用催化剂A能加快相关化学反应速率,但催化剂A并未参与反应
b.在恒温恒压的平衡体系中充入氩气,CH3OH的产率降低
c.当2v(CO)正=v(H2)逆时,反应达到平衡状态
(4)一定温度下,在容积均为2L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。

若甲容器平衡后气体的压强为开始时的![]() ,则该温度下,该反应的平衡常数K=______,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为_____________________________________。
,则该温度下,该反应的平衡常数K=______,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则乙容器中c的取值范围为_____________________________________。
(5)CO与日常生产生活相关。
①检测汽车尾气中CO含量,可用CO分析仪,工作原理类似于燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2-。则负极的电极反应式为__________________。
②碳酸二甲醋[(CH3O)2CO]毒性小,是一种绿色化工产品,用CO合成(CH3O)2CO,其电化学合成原理为4CH3OH+2CO+O2![]() 2(CH3O)2CO+2H2O,装置如图3所示:
2(CH3O)2CO+2H2O,装置如图3所示:
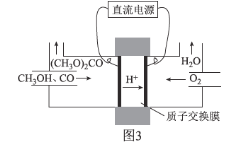
写出阳极的电极反应式:________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com