
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,在碱性溶液中NaClO2比较稳定,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图: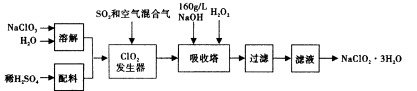
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160 g/L NaOH溶液是指160 g NaOH固体溶于水所得溶液的体积为1L。
(1)160 g/L NaOH溶液的物质的量浓度为____。若要计算该溶液的质量分数,还需要的一个条件是____(用文字说明)。
(2)发生器中鼓入空气的作用可能是____(选填序号)。
a.将SO2氧化成SO3,增强酸性;
b.稀释ClO2以防止爆炸;
c.将NaClO3氧化成ClO2
(3)吸收塔内的反应的化学方程式为____。吸收塔的温度不能超过20℃,其目的是 。
(4)吸收塔中应维持NaOH稍过量,理由是____。
(5)吸收塔中能否用FeCl2代替H2O2____(填能.否)?理由是____。
(6)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是____(选填序号)。
A.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
要得到更纯的NaClO2·3H2O晶体必须进行的操作是____(填操作名称)。
科目:高中化学 来源: 题型:单选题
用某仪器量一液体体积时,平视时读数为nml,仰视时读数为xml,俯视时读数为yml,若x>n>y,则所用的仪器可能是( )
| A.量筒 | B.酸式滴定管 | C.碱式滴定管 | D.容量瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
Ba2+是一种重金属离子,有一环境监测小组欲利用Na2S2O3、KI、K2Cr2O7等试剂测定某工厂废水中Ba2+的物质的量浓度。
(1)在容量瓶的使用方法中,下列操作不正确的是(填字母)________。
| A.使用容量瓶前检查它是否漏水 |
| B.容量瓶用水洗净后,再用待配溶液润洗 |
| C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水至接近标线1~2 cm处,用滴管逐滴滴加蒸馏水至标线 |
| D.配制溶液时,若试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加水至接近标线1~2 cm处,用滴管逐滴滴加蒸馏水至标线 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
化学是一门以实验为主的科学,化学实验是学习探究物质性质的基本方法之一。
(1)下列有关叙述正确的是__________(填写序号)
a.使用托盘天平的第一步操作是将游码移至标尺零刻度处
b.过滤操作过程中,为加快过滤速度可用玻璃棒对漏斗中的溶液进行搅拌
c.用浓硫酸配制稀溶液时,在量筒中衡稀后要冷却至室温再转移到容量瓶中
d.用容量瓶配制溶液时,定容后摇匀液面下降,再加蒸馏水至刻度线处,所得溶液浓度偏低
(2)现有六种气体:H2、O2、NH3、SO2、NO2、NO。可以利用如图所示装置进行收集。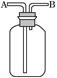
①若气体从B口进入,可收集的气体是_______________;
②若在烧瓶中注满水,则气体应该从______(填写“A”或“B”)口进入,可以收集的气体是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
粗氧化锌中含少量CuO、Fe3O4、SiO2等杂质。工业上以粗氧化锌生产硫酸锌晶体(ZnSO4·7H2O)的工艺流程如下图所示:
已知:常温下,溶液中的Fe3+、Zn2+、Fe2+以氢氧化物形式完全沉淀的pH分别为:3.7,6.5,9.7。
请回答下列问题:
(1)操作③的名称是 ;
(2)加入适量锌粉的作用为 ;
(3)加入30%H2O2反应的离子方程式是 ;
(4)加入适量Ca(OH)2调节溶液pH,促进Fe3+水解,Fe3+水解反应的平衡常数表达式K= ,Ca(OH)2不能过量的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
实验室可用K2Cr2O7固体与浓盐酸混合加热制备氯气(K2Cr2O7被还原为Cr3+)。
(1)K2Cr2O7与浓盐酸反应的化学方程式为_______;若反应中转移3 mol e-,则消耗_______mol K2Cr2O7
(2)稀盐酸与K2Cr2O7固体混合加热没有氯气生成。为探究影响氯气生成的因素,某化学兴趣小组进行如下实验:
①提出假设
假设1:Cl-浓度对反应有影响;
假设2:H+浓度对反应有影响;
假设3: _____________________。
②设计实验方案,进行实验。写出实验步骤及预期现象和结论。
限选举实验试剂:浓盐酸、稀盐酸、浓硫酸、NaOH溶液、K2Cr2O7固体、NaCl固体、湿润的淀粉KI试纸
| 实验步骤 | 预期现象和结论 |
| 步:1:向盛有K2Cr2O7固体的A、B两试管中分别加入一定量的稀盐酸。 | |
| 步骤2: | |
| 步骤3: | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(19分)以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下: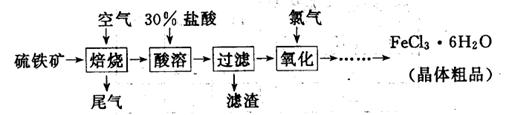
(1)氧化过程中发生反应的离子方程式是 ,检验氧化生成的阳离子的试剂是 。
(2)尾气中主要含N2、O2、SO2和少量的CO2、H2O,取标准状况下的尾气V L测定SO2含量:
方案一:让尾气缓慢通过以下装置。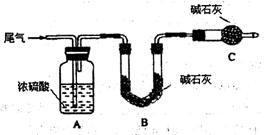
①C仪器的名称是 ,该装置的作用是 。
②实验时先通入尾气,再通入一定量氮气。若通过B装置的增重来测量SO2的体积分数。你认为该方案是否合理 ,请说明理由 (若方案合理该空不必填写)。
方案二:将尾气缓慢通过足量溴水,在所得的溶液中加入过量氯化钡溶液后,过滤,将沉淀洗涤、干燥,称得其质量为m g。
①加入过量氯化钡溶液的目的是 。
②进行沉淀洗涤的方法是 。
③SO2含量的表达式是 (用含m、V的代数式表示)。
(3)从FeCl3溶液中得到FeCl3 6H2O晶体的操作包括 、冷却结晶、过滤,该过程需保持盐酸过量,结合必要的离子方程式说明原因 .
6H2O晶体的操作包括 、冷却结晶、过滤,该过程需保持盐酸过量,结合必要的离子方程式说明原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
K3[Fe(C2O4)3]·3H2O[三草酸合铁(Ⅲ)酸钾晶体]易溶于水,难溶于乙醇,可作为有机反应的催化剂。实验室可用铁屑为原料制备,相关反应过程如下。请回答下列问题: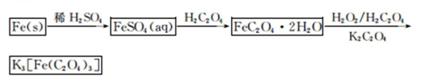
(1)铁屑中常含硫元素,因而在制备FeSO4时会产生有毒的H2S气体,该气体可用氢氧化钠溶液吸收。下列吸收装置正确的是 (填序号)。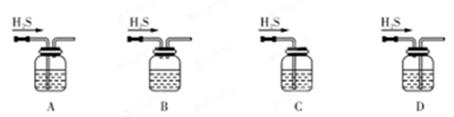
(2)在得到的FeSO4溶液中需加入少量的H2 SO4酸化,目的是 ,得到K3[Fe(C2O4)3]溶液后,加入乙醇的目的是 。
(3)晶体中所含结晶水可通过重量分析法测定,主要步骤有:①称量,②置于烘箱中脱结晶水,③冷却,④称量,⑤重复②~④至恒重,⑥计算。
步骤⑤的目的是 。
(4)C2O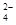 可被酸性KMnO4溶液氧化为CO2气体,故实验产物中K3[Fe(C2O3)3]·3H2O含量测定可用KMnO4标准溶液滴定。
可被酸性KMnO4溶液氧化为CO2气体,故实验产物中K3[Fe(C2O3)3]·3H2O含量测定可用KMnO4标准溶液滴定。
①写出滴定过程中发生反应的离子方程式 。
②下列滴定操作中使滴定结果偏高的是 (填序号)。
| A.滴定管用蒸馏水洗涤后,立即装入标准液 |
| B.锥形瓶在装待测液前未用待测液润洗 |
| C.滴定前滴定管尖嘴处有气泡,滴定后气泡消失 |
| D.读取标准液体积时,滴定前仰视读数,滴定后俯视读数 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室合成乙酸乙酯的步骤如下:
在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。
请回答下列问题:
(1)在烧瓶中除了加入乙酸、浓硫酸和乙醇外,还应放入碎瓷片,目的是__________________。
(2)反应中加入过量的乙醇,目的是________________________________________________。
(3)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加乙酸,边加热蒸馏。这样操作可以提高酯的产率,其原因是_____________________。
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物,下图是分离操作步骤流程图: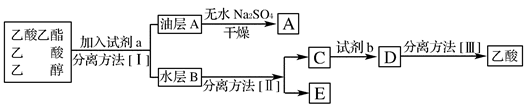
则试剂a是:________,分离方法Ⅰ是:________________________,分离方法Ⅲ是:____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com