


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| B、将标准状况下336 mL氯气通入10 mL 1 mol?L-1的溴化亚铁溶液中:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 |
| C、次氯酸钙溶液中通入过量二氧化硫:Ca(ClO)2+H2O+SO2=CaSO3↓+2HClO |
| D、向澄清石灰水中加入过量的碳酸氢钠溶液:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,两圆圈相交的阴影部分甲、乙、丙表示圆圈内物质相互发生的反应,钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如图所示,两圆圈相交的阴影部分甲、乙、丙表示圆圈内物质相互发生的反应,钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A、甲、乙、丙都属于氧化还原反应 |
| B、丙反应中的氧化剂是Na2O2,还原剂时H2O |
| C、丙反应中消耗1molNa2O2,则转移1mol电子 |
| D、若甲、乙、丙反应后所得溶液的质量分数分别为w1、w2、w3,则:2w1=w2=w3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④ | B、①③⑤⑦ |
| C、④⑧ | D、②④⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、从平衡混合气体中分离出CO2可增大平衡常数K |
| B、平衡后,其他条件不变,加入硫,逆反应速率加快 |
| C、平衡后,若升高温度,CO体积分数增大,则正反应的△H<0 |
| D、平衡后,其他条件不变,通入CO2,该反应的△H减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在20gD216O中含有10NA个电子 |
| B、标准情况下,2.24L己烷所含分子数为0.1NA |
| C、1molCl2参加反应时转移电子数一定为2NA |
| D、含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
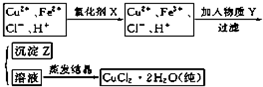
| 溶液中被沉淀的离子 | Fe3+ | Fe2+ | Cu2+ |
| 完全生成氢氧化物沉淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com