
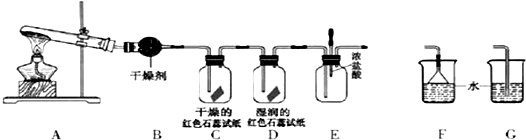
·ÖĪö £Ø1£©ŹµŃéŹŅÖʱø°±ĘųµÄŌĄķŹĒĀČ»Æļ§ŗĶĒāŃõ»ÆøĘ¹ĢĢåŌŚ¼ÓČČĢõ¼žĻĀ·“Ó¦£¬ĖłŅŌøĆ×°ÖĆĢŲµćŹĒ¼ÓČČ¹ĢĢåÖʱøĘųĢåµÄ×°ÖĆ£»
£Ø2£©øł¾Ż·½³ĢŹ½2NH4Cl+Ca£ØOH£©2$\frac{\underline{\;\;”÷\;\;}}{\;}$CaCl2+2NH3”ü+2H2O½įŗĻn=$\frac{m}{M}$”¢v=nvm¼ĘĖć£»
£Ø3£©°±ĘųŅ×ČÜÓŚĖ®£¬ĆܶȱČæÕĘųŠ”£»
£Ø4£©°±ĘųÓėøÉŌļµÄŗģÉ«ŹÆČļŹŌÖ½²»±äÉ«£¬°±ĘųÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶£»
£Ø5£©°±ĘųÓė»Ó·¢µÄHCl»įÉś³É°×ŃĢĀČ»Æļ§¹ĢĢ壻
£Ø6£©ŅņĪŖ°±Ęų¼«Ņ×ČÜÓŚĖ®£¬ĖłŅŌĪüŹÕ°±ĘųŹ±ŅŖÓĆ·Ąµ¹Īü×°ÖĆ£®
½ā“š ½ā£ŗ£Ø1£©øĆ×°ÖĆŹĒ¼ÓČČ¹ĢĢåÖʱøĘųĢåµÄ×°ÖĆ£¬»¹æÉÓĆÓŚÖĘČ”ŃõĘų£¬ČēĀČĖį¼ŲŌŚ¶žŃõ»ÆĆĢµÄ“ß»Æ×÷ÓĆĻĀ¼ÓČČÉś³ÉĀČ»Æ¼ŲŗĶŃõĘų£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2KClO3$\frac{\underline{\;MnO_{2}\;}}{”÷}$2KCl+3O2”ü£®
¹Ź“š°øĪŖ£ŗO2£»
£Ø2£©n£ØNH4Cl£©ØT$\frac{m}{M}$=$\frac{10.7g}{53.5g/mol}$=0.2mol£¬øł¾Ż·“Ó¦·½³ĢŹ½2NH4Cl+Ca£ØOH£©2$\frac{\underline{\;\;”÷\;\;}}{\;}$CaCl2+2NH3”ü+2H2OæÉÖŖ£¬n£ØNH3£©=n£ØNH4Cl£©=0.2mol£¬ĖłŅŌV£ØNH3£©=n•Vm=0.2mol”Į22.4L/mol=4.48L£¬
¹Ź“š°øĪŖ£ŗ4.48£»
£Ø3£©°±ĘųŅ×ČÜÓŚĖ®£¬²»ÄÜÓĆÅÅĖ®·ØŹÕ¼Æ£¬°±ĘųĆܶȱČæÕĘųŠ”£¬ĖłŅŌÓĆĻņĻĀÅÅæÕĘų·ØŹÕ¼Æ£¬
¹Ź“š°øĪŖ£ŗĻņĻĀÅÅæÕĘų·Ø£»
£Ø4£©°±ĘųÓėøÉŌļµÄŗģÉ«ŹÆČļŹŌÖ½²»±äÉ«£¬°±ĘųÓöĖ®Éś³ÉŅ»Ė®ŗĻ°±£¬µēĄė³öµÄĒāŃõøłĄė×ÓÄÜŹ¹ŗģÉ«ŹÆČļŹŌÖ½±äĄ¶£¬ĖłŅŌ°±ĘųÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶£¬ĖłŅŌDÖŠŃÕÉ«·¢Éś±ä»Æ£¬
¹Ź“š°øĪŖ£ŗD£»
£Ø5£©°±ĘųŗĶĀČ»ÆĒā·“Ӧɜ³É¹ĢĢåĀČ»Æļ§£¬½«Į½Ö§·Ö±šÕŗČ”ÅØ°±Ė®ŗĶÅØŃĪĖįµÄ²£Į§°ōææ½ü£¬ÅØ°±Ė®»Ó·¢³öµÄ°±ĘųŗĶÅØŃĪĖį»Ó·¢³öµÄĀČ»ÆĒāĻąÓö·“Ó¦£¬æÉŅŌ¹Ū²ģµ½²£Į§°ōÖ®¼ä³öĻÖ“óĮæ°×ŃĢ£»
¹Ź“š°øĪŖ£ŗÓŠ°×ŃĢÉś³É£»
£Ø6£©ŅņĪŖ°±Ęų¼«Ņ×ČÜÓŚĖ®£¬ĖłŅŌĪüŹÕ°±ĘųŹ±ŅŖÓĆ·Ąµ¹Īü×°ÖĆ£¬Fµ¹æŪµÄĀ©¶·¾ßÓŠĒņŠĪ²æ·ÖĘš»ŗ³å×÷ÓĆ£¬ÄÜ·ĄÖ¹µ¹Īü£¬
¹Ź“š°øĪŖ£ŗF£®
µćĘĄ ±¾Ģāæ¼²éĮĖ°±ĘųµÄŠŌÖŹ·ÖĪöÓ¦ÓĆ£®ŹµŃéŹŅÖʱø·½·Ø£¬×¢ŅāŹµŃ黳±¾²Ł×÷µÄĄķ½āÓ¦ÓĆŗĶ°±ĘųŠŌÖŹµÄŹģĮ·ÕĘĪÕŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017Ń§ÄźÉ½Ī÷Ź”øßŅ»ÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
“ÖŹ³ŃĪ³£ŗ¬ÓŠÉŁĮæK+”¢Ca2+”¢Mg2+”¢Fe3+”¢SO42-µČŌÓÖŹĄė×Ó£¬ŹµŃéŹŅĢį“æNaClµÄĮ÷³ĢČēĻĀ£ŗ
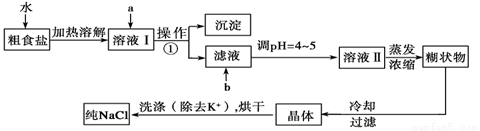
Ģį¹©µÄŹŌ¼Į£ŗ±„ŗĶNa2CO3ČÜŅŗ”¢±„ŗĶK2CO3ČÜŅŗ”¢NaOHČÜŅŗ”¢BaCl2ČÜŅŗ”¢Ba(NO3)2ČÜŅŗ”¢75%ŅŅ“¼”¢ĖÄĀČ»ÆĢ¼”¢Ļ”ŃĪĖį”£
£Ø1£©Óū³żČ„ČÜŅŗIÖŠµÄCa2+”¢Mg2+”¢Fe3+”¢SO42-£¬Ń”³öaĖł“ś±ķµÄŹŌ¼Į£¬°“µĪ¼ÓĖ³ŠņŅĄ“ĪĪŖ___________(Ö»Ģī»ÆѧŹ½)”£
£Ø2£©ČēŗĪ¼ģŃéSO42-ŹĒ·ń³ĮµķĶźČ«_____________”£
£Ø3£©µ÷½ŚpHµÄÄæµÄŹĒ_____________£¬ŹŌ¼ĮbŹĒ________(ĢīĆū³Ę)”£
£Ø4£©Ļ“µÓ³żČ„NaCl¾§Ģå±ķĆęø½“ųµÄÉŁĮæKCl£¬Ń”ÓƵďŌ¼ĮĪŖ______________£¬Ź¹ÓĆøĆŹŌ¼ĮµÄÄæµÄŹĒ³żČ„¾§Ģå±ķĆęµÄŌÓÖŹ£¬¼õÉŁ¾§ĢåµÄĖšŗÄ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
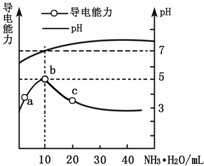 ³£ĪĀĻĀ£¬Ļņ10mL 0.1mol•L-1µÄHRČÜŅŗÖŠÖšµĪµĪČė0.1mol•L-1µÄ°±Ė®£¬ĖłµĆČÜŅŗpH¼°µ¼µēŠŌ±ä»ÆČēĶ¼£®ĻĀĮŠ·ÖĪö²»ÕżČ·µÄŹĒ£Ø””””£©
³£ĪĀĻĀ£¬Ļņ10mL 0.1mol•L-1µÄHRČÜŅŗÖŠÖšµĪµĪČė0.1mol•L-1µÄ°±Ė®£¬ĖłµĆČÜŅŗpH¼°µ¼µēŠŌ±ä»ÆČēĶ¼£®ĻĀĮŠ·ÖĪö²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | bµćČÜŅŗpH=5£¬“ĖŹ±Ėį¼īĒ”ŗĆÖŠŗĶ | |
| B£® | a”«bµćµ¼µēÄÜĮ¦ŌöĒ棬ĖµĆ÷HRĪŖČõĖį | |
| C£® | cµćČÜŅŗ“ęŌŚc£ØNH4+£©£¾c£ØR-£©”¢c£ØOH-£©£¾c£ØH+£© | |
| D£® | b”«cČĪŅāµćČÜŅŗ¾łÓŠc£ØH+£©•c£ØOH-£©=KW=1.0”Į10-14 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓÉŅŅĖįŗĶŅŅ“¼ÖĘŅŅĖįŅŅõ„ | B£® | ÓÉŅŅ“¼ÖĘŅŅĻ© | ||
| C£® | ÓɱūĻ©ÓėäåÖĘ1£¬2-¶žäå±ūĶé | D£® | Óɼױ½Ńõ»ÆÖʱ½¼×Ėį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
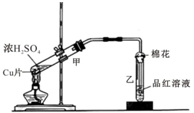 ČēĶ¼ĪŖÅØĮņĖįÓėĶʬ·“Ó¦µÄ×°ÖĆ£®Ēė»Ų“š£ŗ
ČēĶ¼ĪŖÅØĮņĖįÓėĶʬ·“Ó¦µÄ×°ÖĆ£®Ēė»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
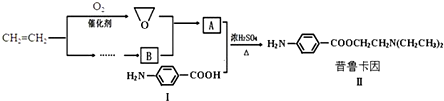

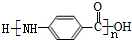 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+”¢Ba2+”¢SO42-”¢Cl- | B£® | Mg2+”¢K+”¢Cl-”¢NO3- | ||
| C£® | H+”¢K+”¢CO32-”¢NO3- | D£® | Ag+”¢Ca2+”¢Cl-”¢HCO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā

 £®
£® £®F1ŗĶF2µÄ¹ŲĻµĪŖĶ¬·ÖŅģ¹¹Ģ壮
£®F1ŗĶF2µÄ¹ŲĻµĪŖĶ¬·ÖŅģ¹¹Ģ壮 £¬¶žĻ©ĢžµÄĶØŹ½ŹĒCnH2n-2£®
£¬¶žĻ©ĢžµÄĶØŹ½ŹĒCnH2n-2£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com