
催化反硝化法可用于治理水中硝酸盐的污染,H2能将NO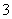 还原为N2。25 ℃时,反应进行10 min,溶液的pH由7变为12,上述反应的离子方程式为________________________________________________________________________
还原为N2。25 ℃时,反应进行10 min,溶液的pH由7变为12,上述反应的离子方程式为________________________________________________________________________
________________________________________________________________________,
其平均反应速率v(NO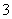 )为________ mol·L-1·min-1。
)为________ mol·L-1·min-1。
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下。下列说法正确的是( )
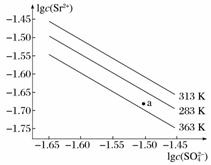
A.温度一定时,Ksp(SrSO4)随c(SO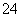 )的增大而减小
)的增大而减小
B.三个不同温度中,313 K时Ksp(SrSO4)最大
C.283 K时,图中a点对应的溶液是饱和溶液
D.283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量的氧化铁杂质。具体实验流程如下:
明矾石

请回答下列问题:
(1)操作1所用到的玻璃仪器的名称是____________。
(2)由溶液3制取氢氧化铝的离子方程式为_______________________________
________________________________________________________________________。
(3)明矾石焙烧时产生SO2,请你写出能验证SO2具有还原性且实验现象明显的化学方程式:______________。
(4)请你写出验证溶液1中有NH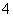 的实验过程:________________________。
的实验过程:________________________。
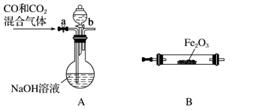
(5)实验室用Fe2O3与CO反应来制取单质Fe。
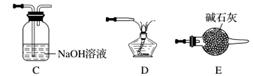
①请按气流由左到右的方向连接下列各装置,顺序为A→________。
②检查装置A气密性的方法是___________________________________________。
③在点燃B处的酒精灯前,应进行的操作是__________________。
④装置C的作用是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,反应N2(g)+O2(g)2NO(g)在密闭容器中进行,回答下列措施对化学反应速率的影响。(填“增大”、“减小”或“不变”)
(1)缩小体积使压强增大:__________;
(2)恒容充入N2:__________;
(3)恒容充入He:__________;
(4)恒压充入He:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,10 mL 0.40 mol·L-1 H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)( )
A.0~6 min的平均反应速率:
v(H2O2)≈3.3×10-2 mol·L-1·min-1
B.6~10 min的平均反应速率:
v(H2O2)<3.3×10-2 mol·L-1·min-1
C.反应到6 min时,c(H2O2)=0.30 mol·L-1
D.反应到6 min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4NH3(g)+5O2(g)4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均反应速率v(X)(反应物的消耗速率或产物的生成速率)可表示为( )
A.v(O2)=0.001 mol·L-1·s-1
B.v(NH3)=0.01 mol·L-1·s-1
C.v(NO)=0.001 mol·L-1·s-1
D.v(H2O)=0.045 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
利用催化剂可使NO和CO发生反应:2NO(g)+2CO(g)2CO2(g)+N2(g) ΔH<0。已知增大催化剂的比表面积可提高化学反应速率。为了分别验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面的表中。
| 实验编号 | T(℃) | NO初始浓度(mol·L-1) | CO初始浓度(mol·L-1) | 催化剂的比表面积(m2·g-1) |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | 1.2×10-3 | 124 | ||
| Ⅲ | 350 | 82 |
(1)请填全表中的各空格;
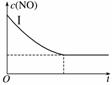
(2)实验Ⅰ中,NO的物质的量浓度(c)随时间(t)的变化如右图所示。请在给出的坐标图中画出实验Ⅱ、Ⅲ中NO的物质的量浓度(c)随时间(t)变化的曲线,并标明各曲线的实验编号。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将a mol·L-1 CH3COONa溶于水配成溶液,向其中滴加等体积的b mol·L-1的盐酸使溶液呈中性(不考虑盐酸和醋酸的挥发),用含a和b的代数式表示醋酸的电离常数Ka=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.硫酸钠溶液和醋酸铅溶液均能使蛋白质变性
B.金属腐蚀的本质是金属原子失电子被氧化的过程
C.工业生产玻璃、水泥、陶瓷,均需要用石灰石为原料
D.人造纤维、合成纤维和光导纤维都是有机高分子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com