
| A�� | ��H2O2�ֽ�����У���Һ��pH���½� | |
| B�� | Fe3+�Ǹ÷�Ӧ�Ĵ��� | |
| C�� | 2H2O��l��+O2��g��=2H2O2��aq����һ���������ܹ��Է����� | |
| D�� | v��H2O2��=2v��O2�� |
���� A���ܷ�ӦΪ2H2O2�T2H2O+O2������Һ��H+Ũ�Ȼ������䣻
B�������ܷ�Ӧ�жϣ�
C��2H2O2�T2H2O+O2�������Է���Ӧ�����淴Ӧ�����Է����У�
D�� ��ͬ�����£���Ӧ����֮�ȵ��ڼ�����֮�ȣ�
��� �⣺A����������Ӧ��ӿɵ�2H2O2=2H2O+O2�������Էֽ�����в����������ӣ�Ҳ�����������ӣ�������Һ�������ӵ�Ũ�Ȼ������䣬����ҺpHֵ���䣬��A����
B���ܷ�ӦΪ2H2O2�T2H2O+O2����Fe2+ΪH2O2�ֽ�Ĵ�����Fe3+���м�����B����
C��2H2O2�T2H2O+O2�������Է���Ӧ�����淴Ӧ�����Է����У���2H2O��l��+O2��g��=2H2O2��aq����һ���������ܹ��Է����У���C����
D����ͬ�����£���Ӧ����֮�ȵ��ڼ�����֮�ȣ���v��H2O2��=2v��O2������D��ȷ��
��ѡD��
���� ���⿼��������ԭ��Ӧ�Լ���������ѧ��Ӧ��̽������Ŀ�Ѷ��еȣ�ע��ӻ��ϼ۵ĽǶȷ���������ԭ��Ӧ�����ܷ�Ӧ������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2H2+O2�T2H2O��H=-2b kJ/mol | B�� | H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=+b kJ/mol | ||
| C�� | 2H2��g��+O2��g���T2H2O��l����H=-2b kJ/mol | D�� | H2O��g���TH2��g��+$\frac{1}{2}$O2��g����H=+b kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ��Һ���ʼ��ԣ�̼��������������ʷ������ڼ� | |
| B�� | ���߾���ϡ���ᷴӦ����CO2����̼�����ƺ����ᷴӦ������ | |
| C�� | �þƾ��Ƽ���ʱ���߾��ɷ����ֽⷴӦ����̼�����Ƹ��ֽ� | |
| D�� | ���߾��ɺͳ���ʯ��ˮ������Ӧ����̼�����Ʒ�Ӧʱ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
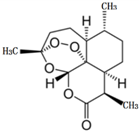 2015��10�£��й�Ůҩѧ���������������Ϳ�űҩ--�����غ�˫�������صĹ��ף���������λ��ѧ�ҹ���2015���ŵ��������ѧ��ҽѧ���������й�����ҽѧ������Ϊֹ��õ����缶����������صļ���ʽ��ѧ�ṹ��ͼ��ʾ������˵������ȷ���ǣ�������
2015��10�£��й�Ůҩѧ���������������Ϳ�űҩ--�����غ�˫�������صĹ��ף���������λ��ѧ�ҹ���2015���ŵ��������ѧ��ҽѧ���������й�����ҽѧ������Ϊֹ��õ����缶����������صļ���ʽ��ѧ�ṹ��ͼ��ʾ������˵������ȷ���ǣ�������| A�� | ���������ڷ��㻯�������H2�����ӳɷ�Ӧ | |
| B�� | ��������������������Һ������Ӧ | |
| C�� | �����صĻ�ѧʽΪC15H22O5 | |
| D�� | �����صĺ˴Ź�����ͼ����12���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ����ͭ | B�� |  �ɰ�����������̼��ˮ�ϳ�̼����� | ||
| C�� |  �ȼҵ | D�� |  ������ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.6mol | B�� | 1mol | C�� | 1.3mol | D�� | 0.8mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1L 1mol/LNaAlO2��Һ�к�����ԭ����Ϊ2NA | |
| B�� | ��״���£�33.6L���������к�����ԭ�ӵ���ĿΪ1.5NA | |
| C�� | 1mol��-14CD3�����������������͵������ֱ�Ϊ11NA��9NA | |
| D�� | ����ͭ�Ĺ����У��������ܽ�32gͭʱת�Ƶĵ�����ΪNA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com