
【题目】苯乙烷(C8H10)可生产塑料单体苯乙烯(C8H8),其反应原理是:C8H10(g)C8H8(g)+H2(g)△H=120kJ·mol-1某温度下,将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,测定不同时间该容器内气体物质的量,得到数据如下表:
时间/min | 0 | 10 | 20 | 30 | 40 |
n(C8H10)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
n(C8H8)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
(1)当反应进行到20min时,该段时间内H2的平均反应速率是。
(2)该温度下,该反应的化学平衡常数是。
(3)若保持其他条件不变,用0.40 mol H2(g)和0.40mol C8H8(g)合成C8H10(g),当有30kJ热量放出时,该反应中H2的转化率是。此时,该合成反应是否达到了平衡状态?(填“是”或“否”)。
(4)工业上以高温水蒸气作为反应体系的稀释剂(不参与反应),C8H10(g)的平衡转化率与水蒸气的用量、体系的温度、压强的关系如图Ⅰ、图Ⅱ所示。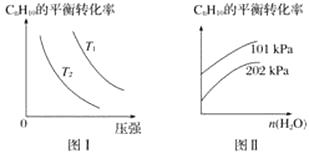
①由图Ⅰ可知,T1T2(填“大于”、“小于”或“等于”)。
②由图Ⅱ可知,当其他条件不变时,水蒸气的用量越大,C8H10的平衡转化率将(填“越大”、“越小”或“不变”),原因是。
【答案】
(1)4×10-3mol.L-1.min-1
(2)0.10
(3)62.5%;否
(4)大于;越大;随着水蒸气的加入,扩大了容器体积,相当于对反应体系减小
压强(或使Q<K),从而使平衡右移,转化率增大。
【解析】I.(1)将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,20min后,剩余0.24mol,减少了0.16mol,
C8H10(g) | C8H8(g)+ | H2(g) | |
起始(mol) | 0.40 | 0 | 0 |
转化(mol) | 0.16 | 0.16 | 0.16 |
20min(mol) | 0.24 | 0.16 | 0.16 |
v(H2)= ![]() =0.004mol/(Lmin);
=0.004mol/(Lmin);
(2)
C8H10(g) | C8H8(g)+ | H2(g) | |
起始(mol/L) | 0.20 | 0 | 0 |
转化(mol/L) | 0.10 | 0.10 | 0.10 |
30min(mol/L) | 0.10 | 0.10 | 0.10 |
化学平衡常数K= ![]() =
= ![]() =0.10;
=0.10;
(3)根据C8H10(g) ![]() C8H8(g)+H2(g),△H=120kJ·mol-1 , 可知 C8H8(g)+H2(g)
C8H8(g)+H2(g),△H=120kJ·mol-1 , 可知 C8H8(g)+H2(g) ![]() C8H10(g) △H=-120kJmol-1 , 有30kJ热量放出时,消耗的H2量为0.25mol,所以氢气转化率=
C8H10(g) △H=-120kJmol-1 , 有30kJ热量放出时,消耗的H2量为0.25mol,所以氢气转化率= ![]() ×100%=
×100%= ![]() ×100%=62.5%;根据(2)知,C8H8(g)+H2(g)
×100%=62.5%;根据(2)知,C8H8(g)+H2(g) ![]() C8H10(g)的平衡常数为
C8H10(g)的平衡常数为 ![]() =10,
=10,
C8H10(g) | C8H8(g)+ | H2(g) | |
起始(mol/L) | 0.25 | 0.25 | 0 |
转化(mol/L) | 0.125 | 0.125 | 0.125 |
某时刻(mol/L) | 0.125 | 0.125 | 0.125 |
![]() =
= ![]() =8≠10,反应不是平衡状态;
=8≠10,反应不是平衡状态;
Ⅱ.(4)①C8H10(g) ![]() C8H8(g)+H2(g)△H=125kJmol-1 , 温度升高,平衡正向移动,C8H10的转化率增大,由图I可知,压强相同时,T1时C8H10的转化率大于T2时C8H10的转化率,故T1大于T2;
C8H8(g)+H2(g)△H=125kJmol-1 , 温度升高,平衡正向移动,C8H10的转化率增大,由图I可知,压强相同时,T1时C8H10的转化率大于T2时C8H10的转化率,故T1大于T2;
②其他条件不变,水蒸气的用量越大,容器的体积越大,相当于减小了原体系的压强,平衡正向移动,转化率增大;
所以答案是:(1)0.004mol/(Lmin);(2)0.10;(3)62.5%;否;(4)①大于;②越大;水蒸气的用量越大,容器的体积越大,相当于减小了原体系的压强,平衡正向移动,转化率增大
【考点精析】本题主要考查了反应速率的定量表示方法和化学平衡状态本质及特征的相关知识点,需要掌握反应速率的单位:mol/(L·min)或mol/(L·s) v=△c-△t;化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)才能正确解答此题.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】现有三组溶液:①含有水份的植物油中除去水份②回收碘的CCl4溶液中的CCl4③用乙醚浸泡青蒿提取其中的有效成份青蒿素 ④除去食盐溶液中的泥沙。分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏、蒸发B.萃取、蒸馏、分液、过滤
C.分液、蒸馏、萃取、过滤D.蒸馏、萃取、分液、蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2 , 在相同温度下发生反应:2SO2+ O2 ![]() 2SO3 , 并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
2SO3 , 并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
A.等于p%
B.大于p%
C.小于p%
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表是元素周期表的一部分,参照元素在表中的位置,请用化学用语回答下列问题:
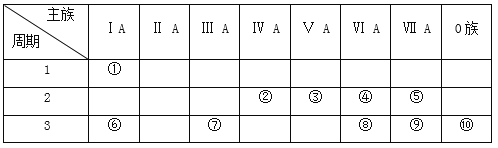
(1)在上述元素最高价氧化物对应水化物中,酸性最强的是_______________,碱性最强的是_____________,显两性的是_____________。(化学式)
(2)这些元素中,化学性质最不活泼原子的原子结构示意图为__________;气态氢化物中,最稳定的是_________(化学式),②③④⑤形成的氢化物中沸点最高的是_______(化学式)。
(3)①和④两种元素的原子按1:1组成的常见化合物的电子式为_____________。
(4)④、⑥、⑦、⑨的简单离子半径由大到小的顺序为______________________________(用离子符号和“>”表示)。
(5)⑥和⑦的最高价氧化物对应水化物之间发生反应的化学方程式_____________________。
(6)为了证明⑥和⑦两种元素的金属性强弱,下列说法或实验能提供证据的是_______。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)——空气燃料电池的工作原理如图所示。电池工作时,下列说法不正确的是
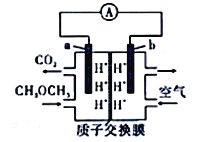
A. b极反应式:O2+H2O+4e-==4OH-
B. a极反应式:CH3OCH3+3H2O-12e-==2CO2↑+12H+
C. b极区溶液的pH变大
D. 每消耗1mol CH3OCH3,有12mol H+向右侧移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应C(s)+H2O(g) ![]() CO(g)+H2(g) ;ΔH >0,下列有关说法正确的是
CO(g)+H2(g) ;ΔH >0,下列有关说法正确的是
A.平衡常数表达式为 ![]()
B.增大体系压强,平衡常数K不发生变化
C.升高体系温度,平衡常数K减小
D.增加C(s)的量,平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将一定量的氨基甲酸铵置于密闭真空容器中(固体体积忽略不计)发生反应:H2NCOONH4(s)![]() 2NH3(g)+CO2(g)△H,达到平衡时测得c(CO2)=amol·L-1。温度不变,达到平衡后压缩容器体积至原来的一半,达到新平衡时测得c(NH3)=xmol·L-1。下列说法正确的是( )
2NH3(g)+CO2(g)△H,达到平衡时测得c(CO2)=amol·L-1。温度不变,达到平衡后压缩容器体积至原来的一半,达到新平衡时测得c(NH3)=xmol·L-1。下列说法正确的是( )
A. 混合气体的平均相对分子质量不再变化时表明达到平衡状态
B. 达到新平衡时,△H为原来的2倍
C. 上述反应达到新平衡状态时x=2a
D. 上述反应体系中,压缩容器体积过程中n(H2NCOONH4)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关电解质的说法正确的是
A.固体NaCl不导电,所以NaCl不是电解质
B.SO3水溶液的导电性很好,所以SO3是电解质
C.液态的铜导电性很好,所以铜是电解质
D.Na2O液态时能导电,所以Na2O是电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com