
关于原子轨道的说法正确的是
A.凡中心原子采取sp3杂化轨道成键的分子其几何构型都是正四面体.
B.CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的
C.sp3杂化轨道是由同一原子中能量相近的s轨道和p轨道混合起来形成的一组能量相等的新轨道
D.凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键.
科目:高中化学 来源:江苏省淮安市2017届高三第三次调研测试化学试卷 题型:选择题
下列指定反应的离子方程式正确的是
A. 向MgCl2溶液中滴加过量氨水:Mg2++2OH-=Mg(OH)2↓
B. 用稀硝酸洗涤试管内壁的银镜:Ag+4H++NO =Ag++NO↑+2H2O
=Ag++NO↑+2H2O
C. 将Cu粉加入到Fe2(SO4)3溶液中:2Fe3++3Cu=2Fe+3Cu2+
D. 向NaAlO2溶液中通入过量CO2:AlO +CO2+2H2O=Al(OH)3↓+HCO
+CO2+2H2O=Al(OH)3↓+HCO
查看答案和解析>>
科目:高中化学 来源:2017届湖北省八校高三第二次联考(3月)理综化学试卷(解析版) 题型:选择题
设NA表示阿伏伽德罗常数的值。下列说法正确的是( )
A. 向含有FeI2的溶液中通入适量氯气,当有1molFe2+被氧化时,该反应转移电子数目为3NA
B. 40gCuO和Cu2S混合物中所含铜原子的数目不等于0.5 NA
C. 含0.1molNH4HSO4的溶液中,阳离子数目略小于0.2NA
D. C3H8分子中的2个H原子分别被1个-NH2和1个-OH取代,1mol此有机物所含共用电子对数目为13NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏银川市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 第一电离能的周期性递变规律是原子半径、化合价、电子排布周期性变化的结果
B. 通常元素的第一电离能为正值,第二电离能为负值
C. 电负性是相对的,所以没有单位
D. 分析元素电负性数值可以看出,金属元素得到电负性较大,非金属元素得到电负性较小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏银川市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列对一些实验事实的理论解释正确的是
选项 | 实验事实 | 理论解释 |
A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
B | CO2为直线形分子 | CO2分子中C=O之间的夹角为180° |
C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省牡丹江市高一3月月考化学试卷(解析版) 题型:简答题
安全气囊是行车安全的重要设施。当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客。为研究安全气囊工作的化学原理,取安全装置中的粉末进行研究。经实验分析,确定该粉末是一种混合物且只含Na、Fe、N、O四种元素。
(1)氧元素在元素周期表中的位置是__________________,Na原子结构示意图为_____________,其中三种主族元素的离子半径从大到小的顺序是___________________(用离子符号表示)。
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类 型是____________________。
型是____________________。
(3)水溶性实验表明,安全气囊中固体粉末部分溶解,不溶物为一种红棕色固体,可溶于盐酸,写出反应的化学方程式_______________________________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省牡丹江市高一3月月考化学试卷(解析版) 题型:选择题
已知R2+核内共有N个中子,R的质量数为A,确定m g R2+中含有电子的物质的量为( )
A.  mol B.
mol B.  mol
mol
C.  mol D.
mol D.  mol
mol
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三第五次摸底考试理综化学试卷(解析版) 题型:简答题
甲醇是重要的化工原料,也是一种优质的燃料。
Ⅰ.甲醇脱氢制取甲醛的原理为CH3OH(g)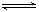 HCHO(g) +H2(g)。某科研小组在2 L密闭容器中充入1 mol CH3OH,对该反应进行了一系列的研究,得到甲醇的平衡转化率随温度的变化曲线如图所示。
HCHO(g) +H2(g)。某科研小组在2 L密闭容器中充入1 mol CH3OH,对该反应进行了一系列的研究,得到甲醇的平衡转化率随温度的变化曲线如图所示。
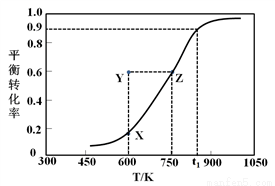
(1)下列选项中,能说明该反应达到平衡状态的是__________;
a.v(CH3OH) =v(HCHO) b.H2的体积分数不再变化
c.甲醛的质量分数不再改变 d.混合气体密度不变
(2)在t1时,该反应的平衡常数为K=________________,此温度下,从反应开始到平衡所经过的时间为5 s,则v(HCHO)为_______mol/(L·min)。向此容器中再通入1.1 mol CH3OH和1.1 mol H2,则平衡向_________(填“正反应”或“逆反应”)方向移动;
(3)600 K时,Y点甲醇的v(正)_______v(逆) (填“>”、“<”或“=”),理由是_____________________;
Ⅱ.已知:CH3OH(g) +CuO(s)=HCHO(g) +Cu(s)+H2O(g) ΔH1=-a kJ/mol;
2Cu(s)+O2(g)=2CuO(s) ΔH2=-b kJ/mol;
(4)则在铜作催化剂时:2CH3OH(g)+O2(g)=2HCHO(g)+2H2O(g) ΔH3=______kJ/mol(用含a,b的代数式表示);
Ⅲ.如图所示是以NaOH溶液为电解质溶液的甲醇燃料电池:
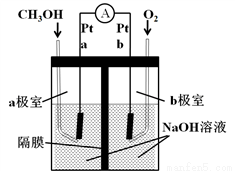
(5)a极电极反应式为__________________________,若隔膜为阴离子交换膜,则电池工作一段后,电池负极区溶液中n(OH-)_____(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2017届山西省太原市高三模拟考试(一)理综化学试卷(解析版) 题型:选择题
茅台酒中存在少量具有凤梨香味的物质X ,其结构如图所示,下列说法正确的是( )
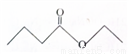
A. X难溶于乙醇
B. X的分子式为C6H10O2
C. 酒中的少量丁酸能抑制X的水解
D. 分子式为C4H8O2且官能团与X相同的物质共有5种(不考虑立体异构)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com