
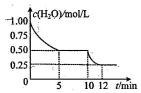
 在2L密闭容器中进行反应C(s)+H2O(g)?CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图.下列判断正确是( )
在2L密闭容器中进行反应C(s)+H2O(g)?CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图.下列判断正确是( )| A. | 0~5min内,v(H2)=0.05mol/(L•min) | |
| B. | 5min时该反应的K值一定小于12min时的K值 | |
| C. | 10min时,改变的外界条件可能是减小压强 | |
| D. | 5min时该反应的v(正)大于11min时的v(逆) |
分析 A.结合v=$\frac{△c}{△t}$计算;
B.若保存温度不变,则K不变,若为绝热容器,温度升高;
C.由图可知,10minc(H2O)减小,该反应为气体体积增大的反应;
D.5~10min为平衡状态,10min~11min,若升高使平衡正向移动,反应速率增大,且正反应速率大于逆反应速率.
解答 解:A.0~5min内,△c(H2O)=0.5mol/L,则△c(H2)=0.5mol/L,可知v(H2)=$\frac{0.5mol/L}{5min}$=0.1mol/(L•min),故A错误;
B.若保存温度不变,则K不变,若为绝热容器,温度升高,该反应为吸热反应,则5min时该反应的K值可能等于或小于12min时的K值,故B错误;
C.由图可知,10minc(H2O)减小,该反应为气体体积增大的反应,则10min时,改变的外界条件可能是减小压强,故C正确;
D.5~10min为平衡状态,10min~11min,若升高使平衡正向移动,反应速率增大,则5min时该反应的v(正)小于11min时的v(逆),故D错误;
故选C.
点评 本题考查浓度随时间的变化曲线,为高频考点,把握图中浓度的变化、K的影响因素、平衡移动为解答的关键,侧重分析与应用能力的考查,注意10min改变的条件为减小压强或升高温度,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A | B | C | D |
 《神农本草经》记载,麻黄能“止咳逆上气” |  84消毒液主要成分是NaClO |  易拉罐主要成分是金属铝 |  贴有该标志的物品是可回收物 |
| 古代中国人已用麻黄治疗咳嗽 | 用于杀菌消毒和衣物的洗涤漂白 | 不可以用氢氧化钠溶液将其溶解 | 废纸、塑料、玻璃、金属均可回收 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
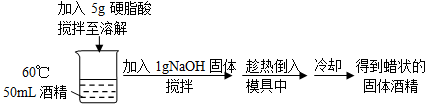
| A. | 将酒精加热到60℃的目的是使更多的硬脂酸溶解在其中 | |
| B. | 上述过程中,有酸碱中和反应发生 | |
| C. | 上述过程中,加入NaOH发生皂化反应 | |
| D. | 常温下,硬脂酸钠在酒精中的溶解度小于在水中的溶解度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 C、N、O、Na、Al、Si、S、Cl是常见的八种元素
C、N、O、Na、Al、Si、S、Cl是常见的八种元素 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
 |  |  |  |
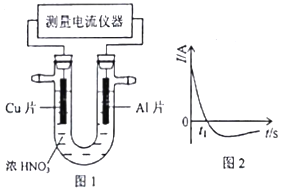
| 用Cl2氧化溶液中的Br- | 分离有机层和水层 | 高温结束后先 停止加热后停止通水 | 贮存液溴 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3,3-二甲基-1-丁烯催化加氢后得到3,3-二甲基-丁烷 | |
| B. | 2-甲基-1,3-丁二烯与Br2的加成产物有3种 | |
| C. | 根据所有原子不在同一平面上可以说明C4H6的某烃是1-丁炔而不是CH2=CH-CH=CH2 | |
| D. | 已知具有单双键交替长链(如:-CH=CH-CH=CH-CH=CH-)的高分子有可能成为导电塑料,故聚乙烯和聚乙炔均可成为导电塑料 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液的溶质质量分数变大 | B. | 溶液仍为饱和溶液 | ||
| C. | 溶液中的Na+数目减小 | D. | 溶液中的c(Na+)增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com