
在以稀硫酸为电解质溶液的铜——锌原电池中,已知其电极反应分别为
锌片:Zn-2e-= Zn2+;铜片:2H+ +2e-= H2↑。下列判断正确的是
A.溶液的酸性逐渐增强
B.铜片逐渐溶解
C.溶液中H+向锌片作定向移动
D.锌片是负极并被氧化
 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:阅读理解
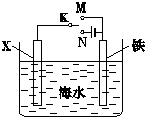 (1)利用如图装置,可以模拟铁的电化学防护.若X为碳棒,为减缓铁的腐蚀,开关K应该置于
(1)利用如图装置,可以模拟铁的电化学防护.若X为碳棒,为减缓铁的腐蚀,开关K应该置于| 实验方法 | 实验现象及结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源:期中题 题型:填空题
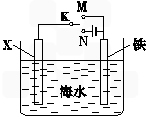
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题


查看答案和解析>>
科目:高中化学 来源: 题型:
(1)以下反应(或过程):①硝酸铵晶体溶于水 ②燃烧天然气 ③生石灰与水反应
④稀盐酸与氢氧化钠溶液反应 ⑤Ba(OH)2·8H2O与氯化铵晶体反应 ⑥锌粒和稀硫酸混合,
其中属于放热反应(或过程)的是 (填序号),写出吸热反应的化学方程式
 。
。
(2)以反应2Fe3+ + Cu=2Fe2++ Cu2+为原理设计一个原电池,
在方框中画出原电池的示意图(在图上标出两极材料、
正负极、电解质溶液和电子流向)。
(3)用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,
能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g)+2N2(g)+6H2(g)![]() Si3N4 (s)+12HCl(g),一定条件下,在密闭恒容的容器中,表示
Si3N4 (s)+12HCl(g),一定条件下,在密闭恒容的容器中,表示
上述反应达到化学平衡状态的是 。
①3υ逆(N2)=υ正(H2) ②υ逆(HCl)=4υ正(SiCl4) ③混合气体的密度保持不变
④c(N2): c(H2): c(HCl)=1:3:6
 ①哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大 ,原因是该反应是 。
①哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大 ,原因是该反应是 。
②哪一时段的反应速率最小 ,原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com