
【题目】已知:H2(g)+F2(g)=2HF(g) △H1=-270kJmol-1。下列说法不正确的是( )
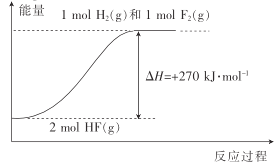
A.1molH2(g)与1molF2(g)的键能之和比2molHF(g)的键能高270kJ·mol-1
B.HF(g)分解为H2(g)与F2(g)的反应过程的能量变化可用如图来表示
C.若反应中有20gHF(g)生成,则放出135kJ热量
D.若H2(g)+Cl2(g)=2HCl(g) △H2=-QkJ·mol-1,则Q<270
【答案】A
【解析】
A.根据△H=反应物的总键能-生成物的总键能,根据反应H2(g)+F2(g)=2HF(g) △H1=-270kJ·mol-1,则反应物1molH2(g)与1molF2(g)的键能之和比生成物2molHF(g)的总键能低270kJ,错误,A符合题意;
B.根据反应,可知2molHF(g)分解生成1molH2(g)和1molF2(g)吸收270kJ热量,可用图示表示,正确,B不符合题意;
C.20gHF(g),其物质的量![]() ,根据反应,生成2molHF(g)放出270kJ热量,现生成1molHF(g),则放出135kJ热量,正确,C不符合题意;
,根据反应,生成2molHF(g)放出270kJ热量,现生成1molHF(g),则放出135kJ热量,正确,C不符合题意;
D.同主族非金属元素的非金属性随着核电荷数的增大而减弱,非金属性越强,气态氢化物的稳定性越强。一般情况下,物质越稳定,具有的能量越低,因此1molH2(g)分别和1molF2(g)、1molCl2(g)反应,由于生成HF(g)更稳定,能量更低,放出的热量更多,则△H2>△H1,Q<270,正确,D不符合题意。
答案选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A、B、C均为短周期元素,它们在周期表中的位置如下图所示。已知:B、C两元素原子最外层电子数之和等于A元素原子最外层电子数的2倍;B.C两元素的核电荷数之和是A元素原子序数的4倍。下列说法正确的是
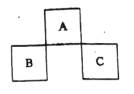
A.C位于元素周期表中第3周期第VA族
B.B的非金属性比A强
C.C的气态氢化物的稳定性比B的强
D.原子半径:r(B)<r(C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将浓度均为0.5molL-1氨水和KOH溶液分别滴入到体积均为20mL且浓度相同的AlCl3溶液中,测得溶液的导电率与加入碱的体积关系如图所示,下列说法中错误的是( )
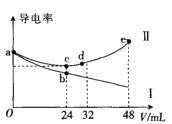
A.AlCl3溶液的物质的量浓度为0.2molL-1
B.根据图象可以确定导电率与离子种类有关
C.cd段发生的反应是Al(OH)3+OH-=AlO2-+2H2O
D.e点时溶液中的离子浓度:c(K+) =c(Cl-) +c(AlO2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列颜色变化与氧化还原无关的是( )
A.湿润的红色布条遇到氯气褪色
B.棕黄色的FeCl3饱和溶液滴入沸水中变红褐色
C.紫色酸性KMnO4溶液通入乙烯气体后褪色
D.浅黄色Na2O2固体露置于空气中逐渐变为白色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据原电池的知识,下列反应可设计成原电池的是( )
A.CH3CH2OH+3O2![]() 2CO2+3H2O
2CO2+3H2O
B.Ba(OH)28H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
C.H2SO4+2NaOH=Na2SO4+2H2O
D.CaO+H2O=Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验在学科中有着非常重要的作用,结合图示实验装置,下列相关分析的描述不正确的是( )
A.图1:盐桥中使用KCl溶液,电子的流向是Zn→G→Cu→CuSO4溶液→盐桥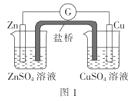
B.图2:可根据该实验验证铁的吸氧腐蚀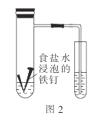
C.图3:在强酸和强碱的中和热实验中,强碱的浓度比强酸的略大
D.图4:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断反应2NO2(g)![]() N2O4(g)是一个放热反应
N2O4(g)是一个放热反应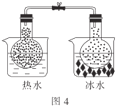
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用相同浓度的NaOH溶液,分别滴定20mL0.1mol·L-1的三种酸(HA、HB和HD)溶液体积的变化曲线如图所示。下列判断正确的是( )
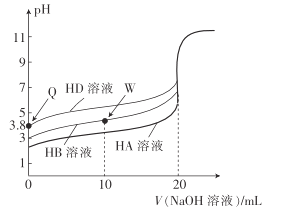
A.由Q点可知,HD的电离平衡常数Ka≈10-7.6
B.三种酸的酸性强弱:HD>HB>HA
C.滴定至W点时,溶液中存在:c(B-)>c(Na+)>c(H+)>c(OH-)
D.当三种溶液恰好完全中和后将其混合,溶液中存在:c(Na+)=c(A-)+c(B-)+c(D-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】开发新型储氢材料是开发利用氢能的重要研究方向。
(1)![]() 是一种储氢材料,可由
是一种储氢材料,可由![]() 和
和![]() 反应制得。
反应制得。
①基态Cl原子中,电子占据的最高电子层符号为 _______,该电子层具有的原子轨道数为 _______。
②Li、B、H元素的电负性由大到小的排列顺序为 ___________。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+ ___________(填“>”“=”或“<”)H-。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如表所示:
|
|
|
|
|
738 | 1451 | 7733 | 10540 | 13630 |
则M是 ______________ (填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代工业生产中常用电解氯化亚铁的方法制得氯化铁溶液吸收有毒的硫化氢气体。工艺原理如下图所示。下列说法中不正确的是( )
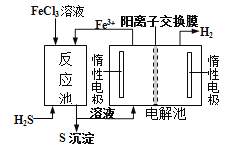
A. H+从电解池左槽迁移到右槽 B. 左槽中发生的反应是:2Cl--2e-=Cl2↑
C. 右槽的反应式: 2H++2e-=H2↑ D. FeCl3溶液可以循环利用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com