
��A��B��C��D����������Ԫ�أ����ǵ�ԭ��������������A����Ȼ�������ԭ��������С��Ԫ�أ�B����Ȼ���к�����ߵ�Ԫ�أ�D������Ȼ���к�����ߵĽ���Ԫ�أ�C��Aͬ���塢��Dͬ���ڡ�
![]() ��д��A��D��Ԫ�ط����������� ������������ ��
��д��A��D��Ԫ�ط����������� ������������ ��
![]() ��A2B�������������� ������������ӻۣ�
��A2B�������������� ������������ӻۣ�
![]() �DZȽ�C��D��ԭ�Ӱ뾶 C�������� D�����>������=��������
�DZȽ�C��D��ԭ�Ӱ뾶 C�������� D�����>������=��������
![]() �ȱȽ�C��D�Ľ�����C������ ���� D�����>������=��������
�ȱȽ�C��D�Ľ�����C������ ���� D�����>������=��������
![]() �ɽ�2.7��D��������200 mL 1 mol?L-1��NaOH��Һ�У��������ɵ������ڱ�״���µ����Ϊ��������
�ɽ�2.7��D��������200 mL 1 mol?L-1��NaOH��Һ�У��������ɵ������ڱ�״���µ����Ϊ��������
![]()
![]()
 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
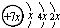 ��B��ͬ���ڵ�һ��������С��Ԫ�أ�C��������������ɵ����ӣ�E����Χ�����Ų�ʽΪ3d64s2���ش��������⣺
��B��ͬ���ڵ�һ��������С��Ԫ�أ�C��������������ɵ����ӣ�E����Χ�����Ų�ʽΪ3d64s2���ش��������⣺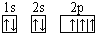

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
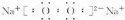
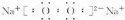
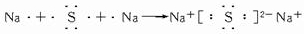
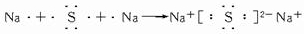
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| I1 | I2 | I3 | I4 | �� |
| 496 | 4562 | 6912 | 9540 | �� |
| ��ѧ�� | F-D | F-F | B-B | F-B | C-D | D-D |
| ����/kJ?mol-1 | 460 | 176 | 347.7 | 347 | 745 | 497.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��5�֣���A��B��C��D����������Ԫ�أ����ǵ�ԭ��������������A����Ȼ�������ԭ��������С��Ԫ�أ�B����Ȼ���к�����ߵ�Ԫ�أ�D������Ȼ���к�����ߵĽ���Ԫ�أ�C��Aͬ���塢��Dͬ���ڡ�
��д��A��D��Ԫ�ط��� �� ��
��A2B���� ������������ӻۣ�
�DZȽ�C��D��ԭ�Ӱ뾶 C D�����>������=��������
�ȱȽ�C��D�Ľ�����C D�����>������=��������
�ɽ�2.7��D��������200 mL 1 mol?L-1��NaOH��Һ�У��������ɵ������ڱ�״���µ����Ϊ��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com