
分析 (1)铁与氢氧化钠不反应,铝与氢氧化钠溶液反应生成可溶性铝盐;
(2)铁与氯化铁发生氧化还原反应生成氯化亚铁;
(3)碳酸钠与二氧化碳和水反应生成碳酸氢钠;
(4)二氧化硅不溶于盐酸,碳酸钙溶于盐酸;
(5)氢氧化铝溶液氢氧化钠,氢氧化镁不溶于氢氧化钠.
解答 解:(1)铝与氢氧化钠溶液反应,离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑;
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)铁与氯化铁发生氧化还原反应生成氯化亚铁,离子方程式:Fe+2Fe3+=3Fe2+;
故答案为:Fe+2Fe3+=3Fe2+;
(3)碳酸钠与二氧化碳和水反应生成碳酸氢钠,离子方程式:CO2+H2O+CO32-=2HCO3-;
故答案为:CO2+H2O+CO32-=2HCO3-;
(4)碳酸钙与盐酸反应离子方程式:CaCO3+2H+=CO2↑+H2O+Ca2+;
故答案为:CaCO3+2H+=CO2↑+H2O+Ca2+;
(5)氢氧化铝与氢氧化钠反应生成偏铝酸钠和水,离子方程式:Al(OH)3+OH-=AlO2-+2H2O;
故答案为:Al(OH)3+OH-=AlO2-+2H2O.
点评 本题考查了物质的除杂及离子方程式的书写,明确除杂的原则:不引人新的杂质,明确离子方程式书写的方法即可解答,题目难度不大.


 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案科目:高中化学 来源: 题型:解答题
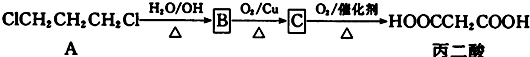

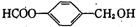 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀.溶液中一定含有大量的SO42- | |
| B. | 加入足量的CaCl2溶液,产生了白色沉淀.溶液中一定有大量的CO32- | |
| C. | 用洁净的铂丝蘸取该溶液,置于火焰上灼烧,透过蓝色钴玻璃能观察到火焰呈紫色.该溶液中一定含有钾离子,可能含有钠离子 | |
| D. | 先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀.溶液中一定含有大量的Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是酸性氧化物,能与NaOH溶液反应 | |
| B. | NH3的水溶液能导电,说明NH3是电解质 | |
| C. | SO2能使溴水褪色,表现了漂白性 | |
| D. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
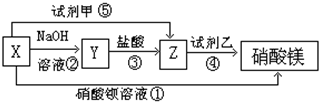
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
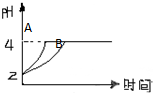 平衡原理探究题
平衡原理探究题| 滴加试剂及量 | 所根据的现象 | 结论 |
| 是盐水解之故 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com