
以下有关原子结构及元素周期律的叙述正确的是( )
|
| A. | 第IA族元素铯的两种同位素137Cs比133Cs多4个质子 |
|
| B. | 同周期元素(除0族元素外)从左到右,原子半径逐渐减小 |
|
| C. | 第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 |
|
| D. | 同主族元素从上到下,单质的熔点逐渐降低 |
| 原子结构与元素周期律的关系;同位素及其应用;同一周期内元素性质的递变规律与原子结构的关系;同一主族内元素性质递变规律与原子结构的关系. | |
| 分析: | 根据同位素的概念,同一周期原子半径的递变规律,同一主族氢化物的稳定性以及单质的熔沸点来解答. |
| 解答: | 解:A、因铯的同位素具有相同的质子数,故A错; B、同周期元素(除0族元素外)从左到右,原子半径逐渐减小,故B对; C、第VIIA族元素从上到下,非金属性在减弱,则其氢化物的稳定性逐渐减弱,故C错; D、第VIIA族元素从上到下,单质的熔点逐渐升高,故D错; 故选:B. |
| 点评: | 本题考查元素周期律,明确常见主族元素的性质是解答的关键,注重基础,一个知识点掌握不好就可能做错,但难度不大. |


科目:高中化学 来源: 题型:
配制250 mL 0.1 mol/L HCl溶液时,下列操作会使配得溶液的物质的量浓度偏大的是( )
A.定容后摇匀,发现液面低于刻度线,再加水至刻度线
B.转移液体后未洗涤烧杯
C.在容量瓶中进行定容时,俯视刻度线
D.配制前洗涤好的容量瓶内有少量水
查看答案和解析>>
科目:高中化学 来源: 题型:
把0.10 mol CH3COONa加到1.0 L 0.10 mol·L-1 CH3COOH溶液中(设加CH3COONa溶液体积不变),求溶液的pH(已知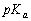 = 4.74)。
= 4.74)。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 18g D2O含有的电子数为10NA
B. 标准状况下,11.2 L SO3中含有的分子数为0.5 NA
C. 7.8 g Na2O2晶体中含有的阴离子数为0.1 NA
D. 常温常压下,44 g CO2气体含有氧原子的个数为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关元素的性质及其递变规律正确的是( )
|
| A. | ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
|
| B. | 第二周期元素从左到右,最高正价从+1递增到+7 |
|
| C. | 同主族元素的简单阴离子还原性越强,水解程度越大 |
|
| D. | 同周期金属元素的化合价越高,其原子失电子能力越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语表示不正确的是 ( )
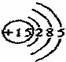 A.P原子的结构示意图:
A.P原子的结构示意图:
B.NaCl的电子式为: 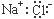
C.HCN分子的结构式:H—C≡N
D.含78个中子的碘的放射性核素: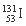
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种元素都是短周期元素,A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne具有相同的电子层排布;5.8 g B的氢氧化物恰好能与100 mL 2 mol・L―1盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构中,最外层电子数是次外层电子数的3倍。根据上述条件回答:
(1)元素C位于第__________周期第__________族,它的最高价氧化物的化学式为____________。
(2)A元素是_________,B元素是________,D元素是_______。(填名称)
(3)A与D形成稳定化合物的电子式是_____________,判断该化合物在空气中是否变质的简单方法是_______________________________。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推断正确的是
A.由H+(aq)+OH-(aq)=H20(1) △H=-57.3 kJ·mol-1,可知含1 mo1 CH3COOH的溶液与含1 mol NaOH的溶液混合,放出热量为57.3 kJ
B.由C(石墨)=C(金刚石) △H=+1.9 kJ·mol-1,可知石墨比金刚石更稳定
C.由N2(g)+3H2(g)=2NH3(g) △H=-92.4 kJ·mol-1,可知将1 mol N2(g)和3 mol H2(g)置于密闭容器中充分反应后放出热量为92.4 kJ
D.由△G=△H-T△S可知,所有的放热反应都能自发进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com