
【题目】碳酸镧[La2(CO3)3]可用于治疗终末期肾病患者的高磷酸盐血症。制备反应原理为:2LaC13+6NH4HCO3= La2(CO3)3↓+6NH4Cl+ 3CO2↑+3H2O;某化学兴趣小组利用下列装置实验室中模拟制备碳酸镧。
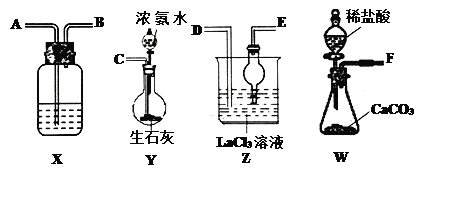
(l)盛放稀盐酸的仪器名称为____________。
(2)制备碳酸镧实验流程中导管从左向右的连接顺序为:F→___→___ →___ →___ →___ 。
(3)Y中发生反应的化学反应式为________________。
(4)X中盛放的试剂是_____,其作用为________________。
(5)Z中应先通入NH3,后通入过量的CO2,原因为_________。
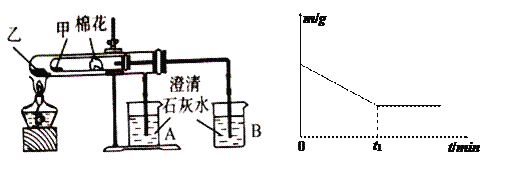
(6)该化学兴趣小组为探究La2(CO3)3和La(HCO3)3的稳定性强弱,设计了如下的实验装置,则甲试管中盛放的物质为_______;实验过程中,发现乙试管中固体质量与灼烧时间的关系曲线如图所示,试描述实验过程中观察到的现象为_______________________。
【答案】 分液漏斗 A B D E C NH3·H2O+CaO= Ca(OH)2+NH3↑或NH3·H2O ![]() NH3+H2O 饱和NaHCO3溶液 除去CO2中的HCl NH3在水的溶解度大 La(HCO3)3 B中澄清石灰水先变混浊,A中后变混浊
NH3+H2O 饱和NaHCO3溶液 除去CO2中的HCl NH3在水的溶解度大 La(HCO3)3 B中澄清石灰水先变混浊,A中后变混浊
【解析】(l)盛放稀盐酸的仪器名称为分液漏斗;正确答案:分液漏斗。
(2)装置W产生二氧化碳,通过装置X除去氯化氢,进入到装置Z中;装置Y产生氨气,进入装置Z中,且要防倒吸,因此要连接E;综上,制备碳酸镧实验流程中导管从左向右的连接顺序为: A →B → D →E → C;正确答案:A B D E C。
(3)Y中为浓氨水与生石灰反应产生氨气,发生反应的化学反应式为NH3·H2O+CaO= Ca(OH)2+NH3↑或NH3·H2O ![]() NH3+H2O;正确答案:NH3·H2O+CaO= Ca(OH)2+NH3↑或NH3·H2O
NH3+H2O;正确答案:NH3·H2O+CaO= Ca(OH)2+NH3↑或NH3·H2O ![]() NH3+H2O。
NH3+H2O。
(4)X中盛放的试剂的作用是为了除去二氧化碳气体中氯化氢气体,需要用饱和NaHCO3溶液;正确答案:饱和NaHCO3溶液;除去CO2中的HCl。
(5)Z中应先通入NH3,后通入过量的CO2,原因为NH3在水的溶解度大,二氧化碳在水中的溶解度较小,但是在氨水中溶解度较大。这样操作可以得到浓度较大的碳酸氢铵溶液,提高反应速率和碳酸镧的产率;正确答案:NH3在水的溶解度大。
(6)一般正盐的稳定性强于对应的酸式盐,所以欲探究La2(CO3)3和La(HCO3)3的稳定性强弱,可以在相同温度下探究两者的稳定性,也可以给正盐更高的温度加热进行探究。若设计题中的实验装置,则甲试管中盛放的物质受热温度较低,应为La(HCO3)3;根据乙试管中固体质量与灼烧时间的关系曲线可知,碳酸镧在一定温度下会发生分解,所以碳酸氢镧一定在更低的温度下发生分解,所以实验过程中可以观察到的现象为B中澄清石灰水先变混浊,A中后变混浊;正确答案:La(HCO3)3;B中澄清石灰水先变混浊,A中后变混浊。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知2H2(g)+O2(g)═2H2O(g)△H=﹣484kJmol﹣1 , 则反应:H2O(g)=H2(g)+1/2O2(g) 的△H为( )
A.─484 kJmol﹣1
B.+484 kJmol﹣1
C.─242 kJmol﹣1
D.+242 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种具有多种药理学活性的黄烷酮类药物。实验室由芳香化合物A制备G的合成路线如下:
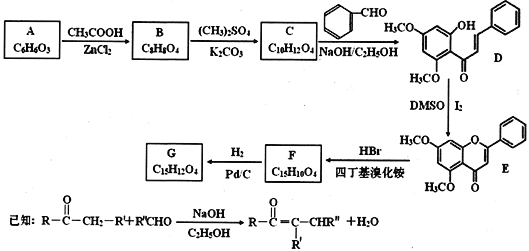
回答以下问题:
(1)A中的官能团名称为________________。E的分子式为________________。
(2)由A生成B和由F生成G的反应类型分别是________________、____________。
(3)由C生成D的化学方程式为____________________。
(4)G的结构简式为____________________。
(5)芳香化合物X是B的同分异构体,可与FeCl3溶液发生显色反应,1molX可与4 mol NaOH反应,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为3:2:2:1。写出一种符合要求的X的结构简式____________。
(6)写出用环戊烯和正丁醛为原料制备化合物![]() 的合成路线(其他试剂任选):__
的合成路线(其他试剂任选):__
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,反应3A(g)+2B(g)![]() 3C(g)+D(g)达到平衡状态的标志是( )
3C(g)+D(g)达到平衡状态的标志是( )
A. 单位时间内, 生成3mol A, 同时消耗3mol C
B. 单位时间内,生成3mol B,同时消耗2mol A
C. A、B、C、D的分子数之比为3:2:3:1
D. A、B、C、D的浓度保持一定
查看答案和解析>>
科目:高中化学 来源: 题型:
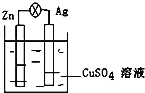
【题目】在银锌原电池中,以硫酸铜为电解质溶液,锌为_____极,电极上发生的是_____反应(“氧化”或“还原”).电极反应式为_____,锌片上观察到的现象为_____银为_____极,电极上发生的是_____反应(“氧化”或“还原”),电极反应式是_____,银片上观察到的现象是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,把试管放入盛有25 ℃饱和石灰水的烧杯中,试管中开始放入几小块镁条,再滴入5 mL的稀盐酸。
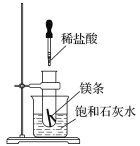
回答下列问题:
(1)实验中观察到的现象是____________________________________________。
(2)产生上述现象的原因是_________________________________________________。
(3)写出有关反应的离子方程式_________________________________________。
(4)由实验推知,MgCl2溶液和H2的总能量______(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入N2和H2 , 在一定条件下使反应N2(g)+3H2(g)2NH3(g)△H<0达到平衡,n(NH3)和n(H2)随时间变化的关系如图所示.下列有关叙述正确的是( ) 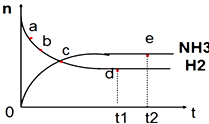
A.c点表示NH3生成速率与NH3分解速率相同
B.c点和e点时反应的平衡常数相同
C.N2的转化率:b>a
D.d点时,n(N2):n(H2):n(NH3)=1:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的盐酸跟过量的锌粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的 ①NaOH溶液 ②H2O ③CH3COONa固体 ④NaNO3溶液⑤稀硫酸
A.②③ B.②④ C.②③④ D.①②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com