
【题目】已知:T℃、P kpa时,容积为V 的密闭容器中充有1molA和2molB,保持恒温恒压使反应达平衡:A(g)+B(g)C(g),平衡时C 的体积分数为40%.
(1)欲保持温度、压强在上述条件下不变,在密闭容器中充入2molA和4molB,则平衡时体系容积为 , C的体积分数为 .
(2)另取一个容积固定不变的密闭容器,仍控制温度为T℃,加入1molB和1molC,要使平衡时C 的体积分数仍为40%,则该密闭容器体积为 .
【答案】
(1)![]() VL;40%
VL;40%
(2)![]() ?VL
?VL
【解析】解:恒温恒压,使反应:A(g)+B(g) ![]() C(g)达到平衡时,C的物质的量分数为40%,(1)温度和压强在上述条件下恒定不变,在密闭容器中充入2mol A和2mol B,2mol:2mol=1mol:1mol,平衡等效,平衡时体积分数与原状态达平衡的体积分数相同, 令转化的物质的量为a,则:
C(g)达到平衡时,C的物质的量分数为40%,(1)温度和压强在上述条件下恒定不变,在密闭容器中充入2mol A和2mol B,2mol:2mol=1mol:1mol,平衡等效,平衡时体积分数与原状态达平衡的体积分数相同, 令转化的物质的量为a,则:
A(g)+ | B(g) | C(g) | |
开始(mol): | 1 | 2 | 0 |
变化(mol) | a | a | a |
平衡(mol) | 1-a | 2-a | a |
则 ![]() ×100%=40%,解得a=
×100%=40%,解得a= ![]() mol,故平衡后反应混合物的总的物质的量为3mol﹣
mol,故平衡后反应混合物的总的物质的量为3mol﹣ ![]() mol=
mol= ![]() mol,
mol,
由于是恒压过程,起始反应物成比例,所以在容器中充入2molA和4molB和容器中充有1molA和2molB时C的体积分数一样仍为40%,所以在密闭容器中充入2molA和4molB,则平衡时体系的总物质的量为 ![]() mol,由同温同压下体积之比等于物质的量之比,则容器的体积VL×
mol,由同温同压下体积之比等于物质的量之比,则容器的体积VL× ![]() mol×
mol× ![]() =
= ![]() VL,
VL,
所以答案是: ![]() VL;40%;(2)容积固定不变的密闭容器,仍然控制温度为T℃,使1molB和1molC反应达到平衡状态时,假设将C完全转化为A和B,A为1mol、B为2mol,C的物质的量分数仍然为40%,所以该容器中反应与初始为等效平衡,所以该装置容器容积与等温等压反应达到平衡后容器体积相等,
VL;40%;(2)容积固定不变的密闭容器,仍然控制温度为T℃,使1molB和1molC反应达到平衡状态时,假设将C完全转化为A和B,A为1mol、B为2mol,C的物质的量分数仍然为40%,所以该容器中反应与初始为等效平衡,所以该装置容器容积与等温等压反应达到平衡后容器体积相等,
1molA和2molB在等温等压条件下发生反应时,设生成的C的物质的量为xmol,
则存在
A(g)+ | B(g) | C(g) | |
开始(mol): | 1 | 2 | 0 |
变化(mol) | x | x | X |
平衡(mol) | 1-x | 2-x | x |
C的体积分数= ![]() =40%,x=
=40%,x= ![]() ,
,
等温等压下,气体的物质的量之比等于其体积之比,所以平衡时气体体积= ![]() =
= ![]() VL
VL
, 因为等效平衡,所以等温等容条件下,该容器容积为 ![]() VL,所以答案是:
VL,所以答案是: ![]() VL.
VL.
【考点精析】认真审题,首先需要了解化学平衡的计算(反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%).


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】向100 mL 0.25 mol·L-1的AlCl3溶液中加入金属钠完全反应,恰好生成只含NaCl和NaAlO2的澄清溶液,则加入金属钠的质量是( )
A.3.45 gB.2.3 gC.1.15 gD.0.575 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示。则下列离子组在对应的溶液中一定能大量共存的是

A. a点对应的溶液中:Na+、OH-、SO42-、NO3-
B. b点对应的溶液中:H+、Fe3+、MnO4-、Cl-
C. c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
D. d点对应的溶液中:S2-、NO3-、Fe2+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是一种重要的化工产品,工业上可以按照下图所示流程生产氨气: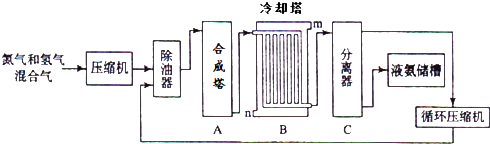
(1)原料气之一氮气的工业制取方法是 , 写出氨气的工业用途(任答一点) .
(2)写出合成塔中发生的反应的化学反应方程式 .
在冷却塔中对混合气体进行冷却,冷水的入口(答m或n).
(3)设备C的作用 .
其分离器中的过程对整个工业合成氨的意义 . (试结合平衡移动原理回答)
(4)在原料气制备过程中混有 CO对催化剂有毒害作用,欲除去原料气中的 CO,可通过如下反应来实现:CO(g)+H2O(g)CO2(g)+H2(g),已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过80%,则起始物中c(H2O):c(CO)不低于(精确到小数点后一位).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,反应2AB (g)+C (g)达到平衡后,升高温度容器内气体密度增大,则下列叙述正确的是( )
A.改变压强对该平衡的移动无影响
B.正反应是放热反应且A不是气态
C.其它条件不变,加入少量A,该平衡向正反应方向移动
D.正反应是吸热反应且A不是气态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列相关离子方程式书写正确的是( )
A.NaClO溶液与FeCl2溶液混合:6Fe2++3ClO﹣+3H2O═2Fe(OH)3↓+3Cl﹣+4Fe3+
B.用食醋检验牙膏中的碳酸钙:CaCO3+2H+═Ca2++CO2↑+H2O
C.FeCl2酸性溶液放在空气中变质:2Fe2++4H++O2═2Fe3++2H2O
D.电解MgCl2水溶液的离子方程式:2Cl﹣+2H2O ![]() H2↑+Cl2↑+2OH﹣
H2↑+Cl2↑+2OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃、2L密闭容器中某一反应不同时刻各物质的量如图(E为固体,其余为气体).回答下列问题:
(1)写出该反应的化学方程式 .
(2)反应开始至3min时,用D表示的平均反应速率为mol/(Lmin).
(3)T℃时,该反应的化学平衡常数K= .
(4)第6min时,保持温度不变,将容器的体积缩小至原来的一半,重新达到平衡后,D的体积分数为 .
物质 | A | B | D | E |
物质的量mol | 0.8 | 1.0 | 0.4 | 0.2 |
(5)另有一个2L的密闭容器,T℃、某一时刻时,容器中各物质的量如表所示:此时v(正)v(逆)(填“大于”或“等于”或“小于”). 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.升高体系的温度或增加某一组分的浓度均能增加反应体系中活化分子所占百分数
B.H2+Cl2 ![]() 2HCl反应中化学能只转变为热能
2HCl反应中化学能只转变为热能
C.面粉生产工厂要求严禁烟火是因为面粉有机物颗粒极小,总表面积巨大容易被引燃爆炸
D.高锰酸钾受热分解是一个熵减小的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下几个热化学方程式,能表示有关物质燃烧时的燃烧热的热化学方程式是( )
A.C(s)+ ![]() O2(g)═CO(g)△H=+110.5 kJ?mol﹣1
O2(g)═CO(g)△H=+110.5 kJ?mol﹣1
B.C(s)+O2(g)═CO2(g)△H=﹣393.5 kJ?mol﹣1
C.2H2(g)+O2(g)═2H2O(l)△H=﹣571.6 kJ?mol﹣1
D.H2(g)+ ![]() O2(g)═H2O(g)△H=﹣241.8 kJ?mol﹣1
O2(g)═H2O(g)△H=﹣241.8 kJ?mol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com