
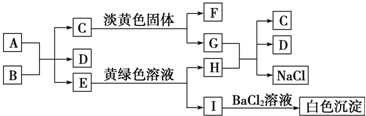
分析 根据图中各物质转化关系,A为固态单质,常温下C、E、F都是无色气体,则A与B的反应应为碳与浓酸硫或浓硝酸的反应,E能与黄绿色溶液(应为氯水)反应,生成I遇氯化钡有白色沉淀,则I中应含有硫酸根,I为H2SO4,H为HCl,所以A与B的反应为碳与浓硫酸的反应,A为C,B为浓H2SO4,E为SO2,D为H2O,C是气体能与淡黄色固体反应,则应为二氧化碳与过氧化钠的反应,所以C为CO2,F为O2,G为Na2CO3,HCl与Na2CO3反应生成二氧化碳、氯化钠和水,符合各物质转化关系,以此解答该题.
解答 解:根据图中各物质转化关系,A为固态单质,常温下C、E、F都是无色气体,则A与B的反应应为碳与浓酸硫或浓硝酸的反应,E能与黄绿色溶液(应为氯水)反应,生成I遇氯化钡有白色沉淀,则I中应含有硫酸根,I为H2SO4,H为HCl,所以A与B的反应为碳与浓硫酸的反应,A为C,B为浓H2SO4,E为SO2,D为H2O,C是气体能与淡黄色固体反应,则应为二氧化碳与过氧化钠的反应,所以C为CO2,F为O2,G为Na2CO3,HCl与Na2CO3反应生成二氧化碳、氯化钠和水,符合各物质转化关系,
(1)依据上述分析可知,C为CO2,固体名称为干冰,F为O2,
故答案为:干冰;O2;
(2)浓硫酸具有强氧化性,在加热条件下可与碳反应,四个反应中A体现强氧化性,B、C体现氧化性和酸性,D体现酸性,故答案为:A;
(3)浓硫酸和碳在加热条件下发生氧化还原反应生成二氧化碳、二氧化硫和水,方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O;
(4)G为Na2CO3,H为HCl,二者反应的离子方程式为CO32-+2H+═CO2↑+H2O,C为CO2,与过氧化钠反应生成碳酸钠和氧气,方程式为2CO2+2Na2O2═2Na2CO3+O2,
故答案为:CO32-+2H+═CO2↑+H2O,2CO2+2Na2O2═2Na2CO3+O2.
点评 本题考查无机物的推断,题目难度中等,物质的颜色为解答该题的突破口,注意把握反应的转化关系的重要信息,侧重于学生分析能力的考查,注意相关知识的学习.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 此时水的电离程度最大 | |
| B. | 溶液中c(NH${\;}_{4}^{+}$)=c(Cl-) | |
| C. | 此时溶液中NH3•H2O的物质的量浓度为$\frac{1}{2}$(a-0.01)mol/L | |
| D. | 用含a的代数式表示NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
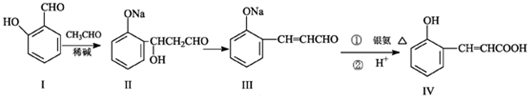
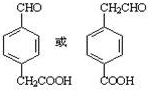 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,CH3OH参与反应的电极为正极 | |
| B. | 放电时,每通入标况下11.2L O2完全反应转移电子数为1mol | |
| C. | 放电时,电解质溶液的pH逐渐增大 | |
| D. | 放电时,负极反应为:CH3OH-6e-+8OH-=CO32-+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将在空气中灼烧呈黑色的铜丝趁热插入盛有乙醇的试管中,铜丝变红色;反复数次,试管中的液体出现刺激性气味,表明乙醇已被铜氧化为乙醛 | |
| B. | 向无水乙醇中加入浓H2SO4,加热至170°C产生的气体通入酸性KMnO4溶液,红色褪去,证明生成的气体全部是乙烯 | |
| C. | 将灼烧后的海带灰加水煮沸2-3分钟的目的是加快碘化物在水中的溶解,使灰烬中的碘离子尽可能多的进入溶液 | |
| D. | 海带中提取碘,可将灰化后的海带加水煮沸一段时间后过滤,在滤液中加入稀硫酸后转移到分液漏斗中用CCl4萃取分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
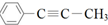 的描述正确的是( )
的描述正确的是( )| A. | 该有机物中只含有非极性键 | |
| B. | 该有机物与溴水的加成产物只有1种 | |
| C. | 该分子中最多有10个原子共平面 | |
| D. | 该分子中最多有5个碳原子共直线 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
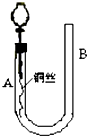 为了说明稀硝酸与铜反应产生无色的一氧化氮气体,某同学设计了如图所示的实验装置.实验时,将分液漏斗的活塞打开,从U形管的长管口B注入稀硝酸,一直到U形管的短管口A单孔塞下沿且液面不再留有气泡为止.关闭活塞,并用酒精灯在U形管短管下微热.当铜丝上有气泡产生时,立即撤去酒精灯.试回答:
为了说明稀硝酸与铜反应产生无色的一氧化氮气体,某同学设计了如图所示的实验装置.实验时,将分液漏斗的活塞打开,从U形管的长管口B注入稀硝酸,一直到U形管的短管口A单孔塞下沿且液面不再留有气泡为止.关闭活塞,并用酒精灯在U形管短管下微热.当铜丝上有气泡产生时,立即撤去酒精灯.试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com