
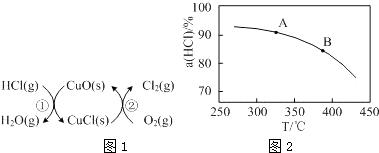
| t��min�� | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n��Cl2��/10?3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
���� ��1����ͼʾ��֪����������Ϊ��4HCl+O2=2Cl2+2H2O����Ӧ������1molCl2��g���ķ�Ӧ��Ϊ��H2����Ӧ�Ȼ�ѧ����ʽΪ��CuCl2��g��+$\frac{1}{2}$O2��g��=CuO��s��+Cl2��g����H2�����ݸ�˹���ɣ���+�ڣ���2�ɵ��ܷ�Ӧ���Ȼ�ѧ����ʽ��
��2������ͼ��֪���¶�Խ�ߣ�ƽ��ʱHCl��ת����ԽС��˵�������¶�ƽ�����淴Ӧ�����ƶ���
������ӦΪ���������С�ķ�Ӧ������ѹǿ��ƽ��������Ӧ�����ƶ�����ͬ�¶���HCl��ƽ��ת���ʱ�֮ǰʵ��Ĵ�
�۸ı��ʩ��������ߦ�HCl��Ӧʹƽ��������Ӧ�����ƶ���ע�ⲻ��ֻ����HCl��Ũ�ȣ�
��3������v=$\frac{��n}{��t}$����2.0��6.0min��v��Cl2��������������֮�ȵ����仯ѧ������֮�ȼ���v��HCl����
��4���������������Ʒ�Ӧ�����Ȼ��ơ����������ˮ���Դ�д����ѧ����ʽ��
��� �⣺��1����ͼʾ��֪����������Ϊ��4HCl+O2=2Cl2+2H2O����Ӧ��Ϊ��2HCl��g��+CuO��s��?H2O��g��+CuCl2��s����H1��
��Ӧ������1molCl2��g���ķ�Ӧ��Ϊ��H2����Ӧ�Ȼ�ѧ����ʽΪ��CuCl2��g��+$\frac{1}{2}$O2��g��=CuO��s��+Cl2��g����H2��
���ݸ�˹���ɣ���+�ڣ���2�ɵ��ܷ�Ӧ���Ȼ�ѧ����ʽ��4HCl��g��+O2��g��=2Cl2��g��+2H2O��g����H=2����H1+��H2����
�ʴ�Ϊ��4HCl��g��+O2��g��=2Cl2��g��+2H2O��g����H=2����H1+��H2����
��2������ͼ��֪���¶�Խ�ߣ�ƽ��ʱHCl��ת����ԽС��˵�������¶�ƽ�����淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ������H��0����ѧƽ�ⳣ����С����K��A����K��B����
�ʴ�Ϊ������K��A����
������ӦΪ���������С�ķ�Ӧ������ѹǿ��ƽ��������Ӧ�����ƶ�����ͬ�¶���HCl��ƽ��ת���ʱ�֮ǰʵ��Ĵ�ѹ�����ʹѹǿ������Ӧ��HCl��T���ߵ�ʾ��ͼΪ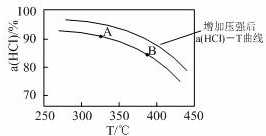 ��
��
�ʴ�Ϊ�� ������ѹǿ��ƽ��������Ӧ�����ƶ�����HCl������ͬ�¶���HCl��ƽ��ת���ʱ�֮ǰʵ��Ĵ�
������ѹǿ��ƽ��������Ӧ�����ƶ�����HCl������ͬ�¶���HCl��ƽ��ת���ʱ�֮ǰʵ��Ĵ�
��A������n��HCl����HClŨ������ƽ�����ƣ���HCl��ת���ʽ��ͣ���A����
B������n��O2��������Ũ������ƽ�����ƣ�HCl��ת������ߣ���B��ȷ��
C��ʹ�ø��õĴ������ӿ췴Ӧ���ʣ����̵���ƽ���ʱ�䣬��Ӱ��ƽ���ƶ���HCl��ת���ʲ��䣬��C����
D����ȥ������H2O��������ƽ�����ƣ�HCl��ת��������D��ȷ��
��ѡ��BD��
��3���⣺��2.0��6.0minʱ���ڣ�HClת�������ʵ���Ϊn����
2HCl��g��+1/2O2��g���TH2O��g��+Cl2��g��
2���������������������� 1
n������������ ��5.4-1.8����10?3mol
��á� n=7.2��10-3mol������v��HCl��=7.2��10-3mol/��6.0-2.0��min�T1.8��10?3mol/min��
��2.0��6.0min����HCl�����ʵ����仯��ʾ�ķ�Ӧ����1.8��10-3mol•min-1��
��4���������������Ʒ�Ӧ�����Ȼ��ơ����������ˮ����Ӧ����ʽΪ2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��
�ʴ�Ϊ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��
���� ����Ƚ��ۺϣ��漰�Ȼ�ѧ����ʽ��д����ѧƽ�⼰ƽ�ⳣ��Ӱ�����ء���ѧ��Ӧ���ʵļ���ȣ���3����ע���õ�λʱ�������ʵ����仯��ʾ�������ϺõĿ���ķ������������������Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CuSO4��Ba��OH��2��Һ��Ӧ��Ba2++SO42-�TBaSO4�� | |
| B�� | AlCl3��Һ�м��������Ũ��ˮ��Al3++4NH3•H2O�TAlO2-+4NH4++2H2O | |
| C�� | ��С�մ�����θ����ࣺHCO3-+H+�TH2O+CO2�� | |
| D�� | �����ƺ������ϣ�CH3COONa+H+�TCH3COOH+Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
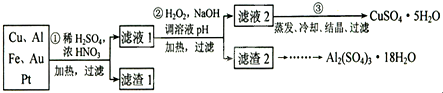
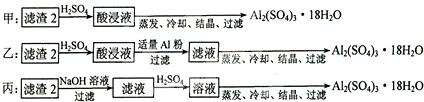
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al | B�� | Na | C�� | Cu | D�� | Fe |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCO3-��ClO-��K+��H+ | B�� | Na+��Fe2+��NO3-��H+ | ||
| C�� | K+��Mg2+��Cl-��SO42- | D�� | OH-��NH4+��Cl-��SO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
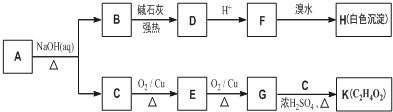
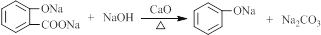 ��
��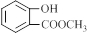 ��
��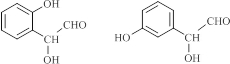 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �� | D�� | �٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ҫ�ɷ�����̼���衢�մɺ�̼��ά���϶��ɵģ��������������ǽ������� | |
| B�� | ��Ѫ�ڷ�Һ������ά����C����Ϊ������ | |
| C�� | ��CO2�ϳɾ�̼�����ɽ������ϣ�����ʵ�֡�̼����ѭ������ | |
| D�� | ����ԺҪ�������Ƹ�����ˮ�ࡢ��̿����ҵ����������������ʵ����̼���á��ľ���ٴ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com