
10gCO和CO2的混合气体在标准状况下的体积是6.72L,则混合气体中CO的体积是多少升?CO2的质量是多少克?
考点: 物质的量的相关计算.
分析: 混合气体的物质的量为:n= =0.3mol,根据质量之和和物质的量之和列式计算.
=0.3mol,根据质量之和和物质的量之和列式计算.
解答: 解:n(CO2)+n(CO)= =0.3mol,
=0.3mol,
n(CO2)×44g/mol+n(CO)×28g/mol=10g,
解之得:n(CO2)=0.1 mol,n(CO)=0.2 mol,
V(CO)=0.2mol×22.4L/mol=4.48L,m(CO2)=0.1mol×44g/mol=4.4g,
答:混合气体中CO的体积是4.48升,CO2的质量是4.4克.
点评: 本题考查学生利用质量和气体的体积进行简单计算,为高频考点,明确质量、体积、物质的量的关系即可解答,难度不大.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
下列有关化学用语使用正确的是()
A. 次氯酸的结构式:H﹣Cl﹣O B. CO2的比例模型 
C. 甲基的电子式: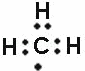 D. 漂粉精的主要成分:CaCl2
D. 漂粉精的主要成分:CaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
|
| A. | 将固体CuO加入稀H2SO4中 CuO+2H+=Cu2++H2O |
|
| B. | 盐酸滴加在石灰石上 CaCO3+2H+=Ca2++H2CO3 |
|
| C. | Ba(OH)2溶液与稀硫酸混合 Ba2++SO42﹣=BaSO4↓ |
|
| D. | 铜片加入稀盐酸中 Cu+2H+=Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是()
A. 密度比为16:11 B. 密度比为11:16
C. 体积比为16:11 D. 原子数比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是()
A. 与28 g CO具有相同分子数的CO2的质量一定是44 g
B. 与V L CO具有相同分子数的CO2,其体积一定是V L
C. 含有相等氧原子数的CO与CO2,其质量之比为28:11
D. 含有相等碳原子数的CO与CO2,其密度之比为21:22
查看答案和解析>>
科目:高中化学 来源: 题型:
2006年4月30日出现的亮菌甲素注射液引起多人中毒死亡的恶性事件.假药生产中原辅料中应有的“丙二醇”被换成廉价而有毒的化工原料“二甘醇”是致病人死亡的重要原因.二甘醇的结构简式是HO﹣CH2CH2﹣O﹣CH2CH2﹣OH.下列有关二甘醇的叙述正确的是()
A. 不能与金属钠发生反应 B. 能发生取代反应
C. 能溶于水,不溶于乙醇 D. 符合通式CnH2nO3
查看答案和解析>>
科目:高中化学 来源: 题型:
某化合物的结构(键线式)及球棍模型如图1,该有机分子的核磁共振波谱图(部分)如图2(单位是ppm).
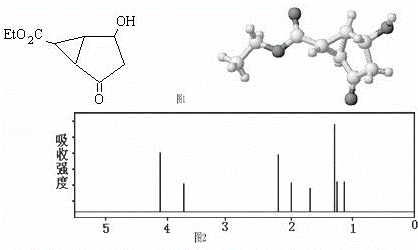
下列关于该有机物的叙述正确的是()
A. 该有机物不同化学环境的氢原子有8种
B. 该有机物属于芳香族化合物
C. 键线式中的Et代表的基团为﹣CH3
D. 该有机物不可能发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 0.1mol/L硫酸铵溶液中各离子的浓度由大到小的顺序是:c (NH4+)>c(SO42﹣)>c(H+)>c(OH﹣)
B. 在苏打与小苏打的混合溶液中存在:c(Na+)+c(H+)=c(OH ﹣)+2c(CO32﹣)+c(HCO3﹣)
C. 在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,证明Na2CO3溶液中存在水解平衡
D. 常温常压下能自发进行的反应,一定都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
有三种不同质量比的氧化铜与炭粉的混合物样品①、②、③.甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中氧化铜的量.
(1)甲取样品①强热,若所得固体为金属铜,将其置于足量的稀硝酸中微热,产生1.12L气体(标准状况),则样品①中氧化铜的质量为 g.
(2)乙取样品②ag强热,生成的气体不能使澄清的石灰水变浑浊.再将反应后的固体与足量的稀硝酸微热,充分反应后,有bg固体剩余,该剩余固体的化学式为C.样品②中氧化铜质量为 g
(以含a、b的代数式表示).
(3)丙称量样品③强热后剩余的固体,质量比原样品减小了cg,若该固体为金属铜,则样品③中氧化铜物质的量(n)的取值范围为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com