【答案】
分析:(1)①氯气是比空气重的可溶于水的气体,依据氯气物理性质和装置分析;
②氯气和水反应生成盐酸和次氯酸;依据平衡状态各物质性质分析判断
③依据氯气具有氧化性能氧化溴离子为溴单质,溴单质在四氯化碳中溶解度大,据此现象分析判断设计实验;
(2)①依据原电池原理和盐桥的作用,在同一烧杯中,电极与溶液含相同的金属元素,设计不同的电极为铜和锌,电解质溶液为硫酸铜和硫酸锌溶液;
②以铜片为电极之一,CuSO
4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,则另一电极应比铜活泼做负极;
③从电硫稳定,能量转化彻底,反应速率快等分析判断;
(3)牲阳极的阴极保护法原理是原电池中把被保护的金属设计成正极,另一活泼的金属做负极.
解答:解:(1)①氯气是比空气中的可溶于水水的有毒气体;
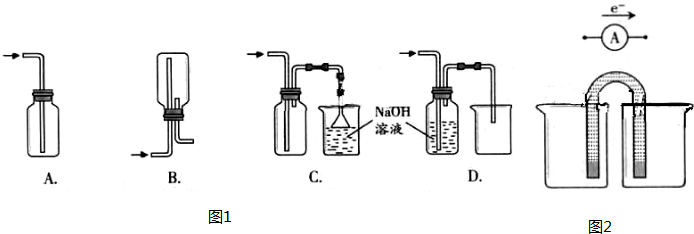
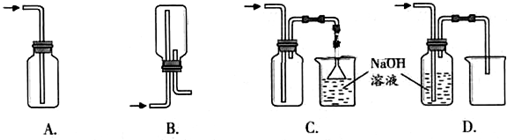
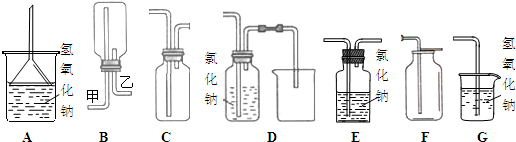
A、导气管位置正确,因为氯气比空气重用向上排气方法,但只有进气口,无出气口,无法排出气体,故A错误;
B、此装置是用来收集比空气轻的气体,若收集氯气,需要短进长出,故B错误;
C、装置长进短出可以收集比空气重的气体氯气,剩余的氯气有毒需要用氢氧化钠溶液吸收,为防止倒吸,用倒扣在水面的漏斗,符合要求,故C正确;
D、氯气通入去海南溶液会发生反应.氯气被氢氧化钠吸收,不能收集到氯气,故D错误;
故答案为:C;
②将Cl
2通入水中,发生反应Cl
2+H
2O=HCl+HClO,所得溶液中具有氧化性的含氯粒子为Cl
2 HClO ClO
-;
故答案为:Cl
2、HClO、ClO
-;
③氯气具有氧化性能氧化溴离子为溴单质,溴单质在四氯化碳中溶解度大,可以加入溴化钠溶液,充分振荡反应,Cl
2+2Br
-=2Cl
-+Br
2,静置后溴溶于下层的四氯化碳层呈橙色;
故答案为:加入适量的NaBr溶液,充分振荡,静置.溶液分层,同时下层液体颜色为橙色;
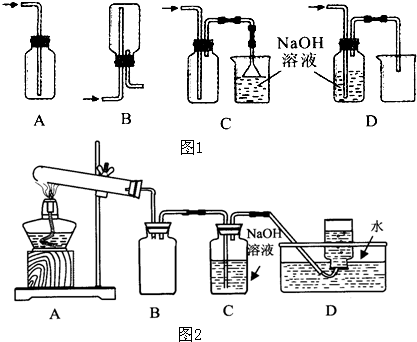
(2)①在同一烧杯中,电极与溶液含相同的金属元素,如图示设计原电池,锌做负极,铜做正极,原电池的甲装置示意图为:
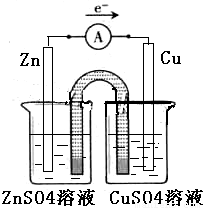
故答案为:
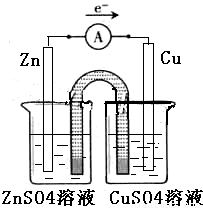
;
②以铜片为电极之一,CuSO
4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,依据原电池反应的原理,需要选用比铜活泼的锌做负极,下层原电池,负极发生氧化反应,Zn-2e
-=Zn
2+,锌溶解,故答案为:溶解;
③甲乙两种原电池中可更有效地将化学能转化为电能的是甲,因为甲可以保持电流稳定,化学能基本都转化为电能.而乙中的活泼金属还可以与CuSO
4溶液发生置换反应,部分能量转化为热能,故答案为:甲,甲可以保持电流稳定,化学能基本都转化为电能.而乙中的活泼金属还可以与CuSO
4溶液发生置换反应,部分能量转化为热能;
(3)根据牺牲阳极的阴极保护法原理,是原电池原理的应用,利用被保护的金属做正极被保护选择,为减缓电解质溶液中铁片的腐蚀,应选择比铁活泼的金属做负极,在电池内电路为阳极,称为牺牲阳极的阴极保护法,材料中 选择锌做阳极,故答案为:Zn.
点评:本题考查了气体收集方法,离子检验试验设计,原电池装置设计,盐桥的作用分析应用,金属保护的方法和名称,题目难度中等.

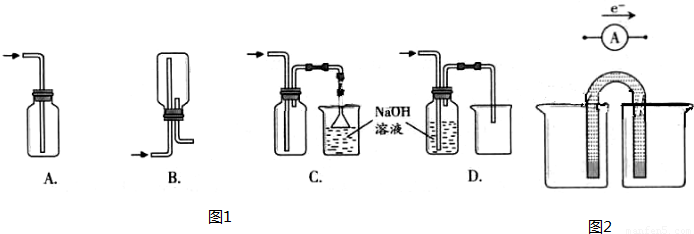

 ;
;

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案