
短周期金属元素甲~戊在元素周期表中的相对位置如下表所示。下列判断正确的是( )
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
A.原子半径:丙<丁<戊
B.金属性:甲>丙
C.氢氧化物碱性:丙>丁>戊
D.最外层电子数:甲>乙
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:
某有机物的结构简式为
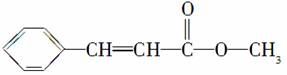 ,由此推测它最不可能具有的性质是( )
,由此推测它最不可能具有的性质是( )
A.能发生水解反应
B.能被新制Cu(OH)2氧化
C.能使溴水褪色
D.能加聚得高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z为元素周期表相邻的三种短周期元素,X和Y同周期,Y和Z同主族。三种元素原子的最外层电子数之和为17,核内质子数之和为31,则X、Y、Z是( )
A.Mg、Al、Si B.Li、Be、Mg
C.N、O、S D.P、S、O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.处于最低能量的原子叫做基态原子
B.3s2表示3s能级有两个轨道
C.同一原子中,1s、2s、3s电子的能量逐渐减小
D.同一原子中,3d、4d、5d能级的轨道数依次增多
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z三种元素的原子,其最外层电子排布分别为ns1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是( )
A.XYZ2 B.X2YZ3
C.X2YZ2 D.XYZ3
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)A、B、C、D、E、F是元素周期表前四周期的元素,它们在元素周期表中的位置如图所示:
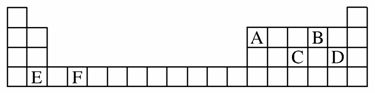
①写出F的基态原子的核外电子排布式:___________________________________________
________________________________________。
②C元素的第一电离能比同周期相邻的两种元素的第一电离能都高的原因是____________________。
(2)A、B、C 3种元素中,A的第一电离能最小,C的电负性最大,3种元素的失电子能力由强到弱的顺序为
___________________________________________。
(3)D、E两种元素形成的化合物化学式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是( )
A.乙烯分子里C、H原子都处在同一平面上,而乙烷分子里的C、H原子不处在同一平面上
B.乙烯和乙烷都能在空气中燃烧而被O2氧化,具有强还原性,所以它们也能被强氧化剂KMnO4氧化
C.相同质量的乙烯和乙炔分别在足量的O2中完全燃烧,乙炔消耗的O2少
D.若要制取一氯乙烷,最好采用乙烯与HCl加成,而不宜采用乙烷与Cl2光照取代生成
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某有机物X的结构简式为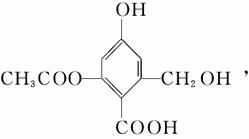 下列有关叙述不正确的是 ( )。
下列有关叙述不正确的是 ( )。
A.1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol
B.X在一定条件下能与FeCl3溶液发生显色反应
C.X在一定条件下能发生消去反应和酯化反应
D.X的化学式为C10H10O6
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验中,溶液颜色有明显变化的是( )
A.少量明矾溶液加入到过量NaOH溶液中
B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液
C.少量Na2O2固体加入到过量NaHCO3溶液中
D.在酸性高锰酸钾溶液中滴入少量Fe2(SO4)3稀溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com