
X��Y��Z��M��G����Ԫ�ط�������������,��ԭ��������������X��Zͬ����,���γ����ӻ�����ZX ; Y��Mͬ����,���γ�MY2��MY3���ַ��ӡ�
��1��Y��Ԫ�����ڱ��е�λ��Ϊ���������������� ��
��2������Ԫ�ص�����������Ӧ��ˮ����������ǿ������������ (д��ѧʽ),�ǽ�����̬�⻯�ﻹԭ����ǿ������������ (д��ѧʽ)��
��3��X��Y��Z��M��������ε���Һ��Ӧ�ɲ���MY2���壬д���䷴Ӧ���ӷ���ʽ������������������
��4��M����������G�ĵ��ʵ�ˮ��Һ����Ư���ԣ���ͬ�����£���ͬ�����M����������Y�ĵ��ʻ��ͨ��Ʒ����Һ��Ʒ����Һ������������ɫ����ɫ����ԭ���û�ѧ����ʽ��ʾ������������������
��1���ڶ�����VIA�� ��2��HClO4 H2S ��3��HSO3-+H+ = SO2��+ H2O
��4������ɫ �� Cl2+SO2 +2H2O =H2SO4 +2HCl
��������
�����������1���������֪X��H��Y��O��Z��Na��M��S��G��Cl����Y��Ԫ�����ڱ��е�λ����λ�ڵڶ�����VIA�壬��2�����ڷǽ�������ǿ��Ԫ����Cl������������������Ӧ��ˮ����������ǿ����HClO4���ǽ�����̬�⻯�ﻹԭ����ǿ����H2S����3��MY2ΪSO2����������Ԫ����ɵ���������ΪNaHSO4��NaHSO3 ��NaHSO4��ˮ��Һ�пɵ����H+��һԪǿ������ã���Ӧ�����ӷ���ʽΪ��HSO3-+H+ = SO2��+ H2O ����4�� )M����Ư���Ե�������ΪSO2��G�ĵ���ΪCl2����ΪSO2�л�ԭ�� ��Cl2�������ԡ�������1:1�����ʵ����ıȻ�ϣ���ˮ�з���ǡ��������ԭ��ӦCl2+ SO2+ 2H2O=2HCl+H2SO4������û��Ư���Ե�HCl��H2SO4�����ʧȥƯ��������
���㣺����Ԫ�ص��ƶϼ�SO2��Cl2��Ư���ԡ�H2S��ԭ�Ե����ʵ�֪ʶ��


 ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д� Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
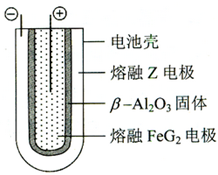 ��2012?���X��Y��Z��M��G����Ԫ�ط������������ڣ���ԭ��������������X��Zͬ���壬���γ����ӻ�����ZX��Y��Mͬ���壬���γ�MY2��MY3���ַ��ӣ�
��2012?���X��Y��Z��M��G����Ԫ�ط������������ڣ���ԭ��������������X��Zͬ���壬���γ����ӻ�����ZX��Y��Mͬ���壬���γ�MY2��MY3���ַ��ӣ�

| ��� | �ŵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�




�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�����ʡ��������У��һ������������ѧ�Ծ����������� ���ͣ��ƶ���
X��Y��Z��M��G����Ԫ�ط������������ڣ���ԭ��������������X��Zͬ��
�壬���γ����ӻ�����ZX,Y��Mͬ���壬���γ�MY2��MY3���ַ��ӡ���ش��������⣺
(1)Y��Ԫ�����ڱ��е�λ��Ϊ ��
(2)����Ԫ�ص�����������Ӧ��ˮ����������ǿ���� ��д��ѧʽ����
�ǽ�����̬�⻯�ﻹԭ����ǿ���� ��д��ѧʽ����
(3)X2M��ȼ���ȡ�H��-a kJ��mol-1��д��X2Mȼ�շ�Ӧ���Ȼ�ѧ����ʽ�� ��
(4)ZX�ĵ���ʽΪ ��ZX��ˮ��Ӧ�ų�����Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com