
有电解装置如图所示.B装置盛1L 2mol/L AgNO3溶液.通电后,润湿的淀粉KI试纸的C装置中a端变蓝色.电解一段时间后,试回答:

(1)A中发生的化学反应方程式为________.
(2)在B中观察到的现象是________.
(3)室温下,若从电解开始到时间为t时,A,B装置中共收集到气体0.168L(标准状况),若电解过程中无其他副反应发生,且溶液体积变化忽略不计,则在t时,A溶液的pH为________.
科目:高中化学 来源:学习周报 化学 人教课标高二版(选修4) 2009-2010学年 第18期 总第174期 人教课标版(选修4) 题型:022
工业上用纯净的氧化铝为原料,采用电解的方法制铝.冶炼的主要设备是一个呈长方形的电解槽.电解槽的外面是钢壳,内衬耐火砖作为绝缘和保护层.用碳作槽底,底部的碳块跟它下部的钢导电棒相连接,槽中有带有导电杆的两排碳块,中间是熔融冰晶石
(Na3AlF6,它是Al2O3的“熔剂”,在1000℃左右就可以得到熔融Al2O3)和氧化铝(Al2O3)的熔融体.其电解装置如图所示:
(1)电解槽中阳极材料是________,阴极材料是________.
(2)工业冶炼铝的原理用电极反应式可表示为________.
(3)电解冶炼铝的过程中,除了定期补充氧化铝外,还要定期补充________,这样做的理由是________.
(4)氯化铝的熔点只有190℃,但不用电解熔融AlCl3来制铝,其理由是________.
(5)工业冶炼镁,不是电解熔融MgO,而是电解熔融MgCl2,理由是________.
查看答案和解析>>
科目:高中化学 来源: 题型:

(1)A中发生反应的化学方程式为________________________________________________。
(2)在B中观察到的现象是_______________________________________________________。
(3)室温下,若从电解开始到时间为t时,A、B装置中共收集到气体
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江西省宜春市高三上学期第五次月考理综化学试卷(解析版) 题型:填空题
某种碳酸锰矿的主要成分有MnCO3 、MnO2、FeCO3、MgO、SiO2、Al2O3等。已知碳酸锰难溶于水。一种运用阴离子膜电解法的新技术可用于从碳酸锰矿中提取金属锰,流程如下:
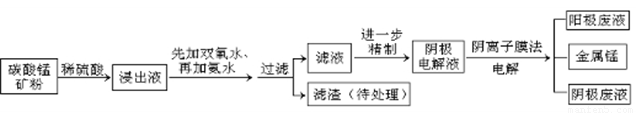
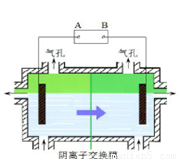
阴离子膜法电解装置如图所示:
(1)写出用稀硫酸溶解碳酸锰反应的离子方程式 。
(2)在浸出液里锰元素只以Mn2+的形式存在,且滤渣中也无MnO2,请解释原因 .
(3)(5分)已知不同金属离子生成氢氧化物沉淀所需的pH如下表:
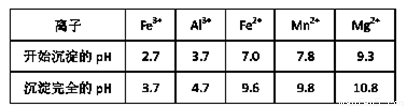
加氨水调节溶液的pH等于6,则滤渣的成分是 ,滤液中含有的阳离子有H+和 。
(4)电解装置中箭头表示溶液中阴离子移动的方向,则A电极是 极。实际生产中,阳极以稀硫酸为电解液,阳极的电极反应式为 。
(5)该工艺之所以采用阴离子交换膜,是为了防止Mn2+进入阳极区发生副反应生成MnO2造成资浪费,写出该副反应的电极反应式 。
查看答案和解析>>
科目:高中化学 来源:2014届河北省唐山市高三年级摸底考试理综化学试卷(解析版) 题型:填空题
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将甲烷燃料电池作为电源进行氯化镁溶液龟解实验,电解装置如图所示。
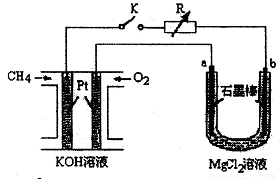
请回答下列问题:
(1)甲烷燃料电池负极的电极反应式为: 。
(2)闭合开关K后,a、b电极上均有气体产生,其中a电极上的气体可用 检验,b电极上得到的气体是 ,电解氯化镁溶液的离子方程式为 。
(3)若甲烷通入量为1.12 L(标准状况),且反应完全,则理论上通过电解池的电子的物质的量为 ,产生的氯气体积为 L(标准状况)。
(4)已知常温常压下,0.25molCH4完全燃烧生成CO2和H2O时,放出222.5kJ热量,请写出CH4燃烧热的热化学方程式 。
已知;①C(石墨)+O2(g)=CO2(g)△H1=-393.5kJ/mol
②2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ/mol
计算:C(石墨)与H2(g)反应生成1molCH4(g)的△H= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com