
| A. | 铜锌原电池中铜是正极 | |
| B. | 用电解法电解氯化钠溶液时,铜可作阴极 | |
| C. | 用电解法精炼粗铜时粗铜作阴极 | |
| D. | 在镀件上电镀铜时可用金属铜作阳极 |
分析 A.铜锌原电池中,锌易失电子而作负极,铜作正极;
B.用铜作阳极电解氯化钠溶液时,阳极上铜失电子生成铜离子;
C.电解精炼粗铜时,粗铜作阳极;
D.电镀时,镀层作阳极,镀件作阴极.
解答 解:A.铜锌原电池中,锌易失电子发生氧化反应而作负极,铜作正极,正极上得电子发生还原反应,故A正确;
B.用铜作阳极电解氯化钠溶液时,阳极上铜失电子而不是电解质溶液中氯离子失电子,所以得不到氯气,所以粗铜作阴极,故B正确;
C.电解精炼粗铜时,粗铜作阳极,纯铜作阴极,故C错误;
D.电镀时,镀层作阳极,镀件作阴极,所以在镀件上电镀铜时,铜作阳极,镀件作阴极,故D正确;
故选C.
点评 本题考查了原电池和电解池原理,明确各个电极上得失电子是解本题关键,易错选项是C,注意活泼金属作电解池阳极时,金属失电子而不是溶液中阴离子失电子,为易错点.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:选择题
| A. | M、N的简单离子半径:r(N-)>r(M2-) | |
| B. | 气态氢化物的稳定性:M>X | |
| C. | X、Y形成的化合物中只有离子键 | |
| D. | X、Y、N所形成化合物的水溶液可能显中性或碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子数为NA的CO、N2混合气体的质量为28g | |
| B. | 0.1mol氧气作为氧化剂得到电子的数目一定为0.4NA | |
| C. | 22.4L氯气和氮气的混合气体含有2NA个原子 | |
| D. | 0.1mol•L-1的氢氧化钠溶液含有0.1NA个OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l);△H=-1135.7 kJ/mol | |
| B. | 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=-1000.3 kJ/mol | |
| C. | N2H4(g)+NO2(g)=3/2N2(g)+2H2O(l);△H=-1135.7 kJ/mol | |
| D. | 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=-1135.7 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 电解时,石墨作阴极,不锈钢作阳极 | |
| B. | 电解时,阳极反应是:I--6e-+3H2O=IO3-+6H+ | |
| C. | 溶液调节至强酸性,对生产有利 | |
| D. | 电解前后溶液的pH几乎不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 被昆虫叮咬以后,因有少量蚁酸而使皮肤红肿,可涂抹一些稀氨水或肥皂水消肿 | |
| B. | 用新制的Cu(OH)2与病人尿液共热,可检验尿中是否含有葡萄糖 | |
| C. | 可用FeCl3溶液检验某工厂废水中是否含有苯酚 | |
| D. | 铜和铝都有良好的导电性,所以电工操作时可将铜线和铝线绞接 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
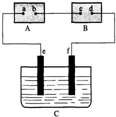 图中A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,C为盛有稀硫酸的电解槽,e、f为铂电极.接通电路后,发现B上的c点显红色.试回答:
图中A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,C为盛有稀硫酸的电解槽,e、f为铂电极.接通电路后,发现B上的c点显红色.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,1mol 任何物质的体积约为22.4L | |
| B. | 22.4L氮气的物质的量一定是1mol | |
| C. | 在标准状况下0.5mol 氢气和氧气的混合气体的总体积约为11.2L | |
| D. | 如果1mol气体的体积为22.4L,则这些气体一定处于标准状况 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XO3-中X为+5价,故X元素位于第VA族 | |
| B. | X位于第二周期第VIIA族 | |
| C. | X可能是氯元素 | |
| D. | X可能是氮元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com