
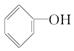
 B.
B.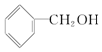 C.CH3 CH2-O-CH2CH3 D.CH3 OH E.CH3-O-CH3 F.HO-CH2CH2-OH
C.CH3 CH2-O-CH2CH3 D.CH3 OH E.CH3-O-CH3 F.HO-CH2CH2-OH分析 (1)乙醇密度比水小;
(2)乙烯中含双键可和水发生加成反应生成乙醇;
(3)根据同系物及同分异构体的概念分析;
(4)乙醇含有羟基,可发生催化氧化,可燃烧,可发生取代反应和消去反应,以此解答该题.
解答 解:(1)乙醇的密度比水小,故答案为:小;
(2)乙烯中含双键可和水发生加成反应生成乙醇,反应方程式为:CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,
故答案为:CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH;
(3)结构相似,在组成上相差若干个CH2原子团的物质互称同系物,故乙醇的同系物为:甲醇;
分子式相同结构不同的有机物互称同分异构体,故乙醇的同分异构体为甲醚;
故答案为:D;E;
(4)①乙醇在铜做催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
②46g乙醇的物质的量为:$\frac{46g}{46g/mol}$=1mol,C2H5OH+3O2$\stackrel{点燃}{→}$2CO2+3H2O,所用1mol乙醇燃烧消耗3mol氧气,
故答案为:3;
③A.乙醇含有羟基,能和酸性高锰酸钾溶液发生氧化还原反应,故A错误;
B.实验室制乙烯时,温度控制在170℃,故B错误;
C.黄酒中某些微生物将乙醇氧化为乙酸,乙酸具有酸性,于是酒就变酸了,故C正确
D.陈年的酒很香是因为乙醇和乙醇被氧化生成的乙酸发生酯化反应生成乙酸乙酯,乙酸乙酯具有香味,故D正确.
故答案为:CD.
点评 本题考查有机物的结构和性质,涉及乙醇的工业生产、催化氧化反应以及与乙酸发生的酯化反应等知识,为高考常见题型和高频考点,掌握有机反应的断裂化学键和形成化学键的情况(反应机理)是解题的关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
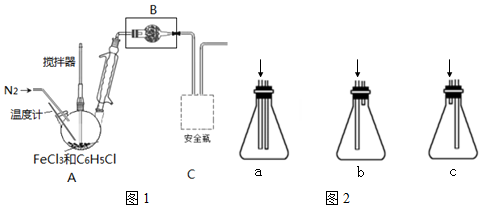
| C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl、C6H4Cl2、苯,易吸水. | ||
| 熔点/℃ | -45 | 53 | -- | -- |
| 沸点/℃ | 132 | 173 | -- | -- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60 mL 0.03 mol•L-1HCl溶液 | B. | 60 mL 0.04 mol•L-1KCl溶液 | ||
| C. | 20 mL 0.03 mol•L-1CaCl2溶液 | D. | 50 mL 0.05 mol•L-1AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当Al3+恰好完全沉淀时,消耗Ba(OH)22 mol | |
| B. | 当SO42-恰好完全沉淀时,Al3+全部转化为Al(OH)3 | |
| C. | 当向溶液中加入1.5mol Ba(OH)2时,反应可用下列离子方程式表示:2Al3++3 SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| D. | 随着加入的Ba(OH)2的物质的量不断增大,沉淀的物质的量不断增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 显蓝色的淀粉溶液中通入足量的SO2后变成无色溶液:I2+SO2+2H2O═2I-+SO42-+4H+ | |
| B. | 向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | 碳酸氢钙溶液中滴加氢氧化钠溶液至Ca2+恰好完全沉淀:Ca2++HCO3-+OHˉ═CaCO3↓+H2O | |
| D. | 盛放烧碱溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3溶液(FeCl2):通入适量Cl2 | |
| B. | Fe2O3固体(Al2O3):加入烧碱溶液,过滤 | |
| C. | Cl2气体(HCl):通过NaOH溶液洗气后干燥 | |
| D. | Na2CO3固体(NaHCO3):加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
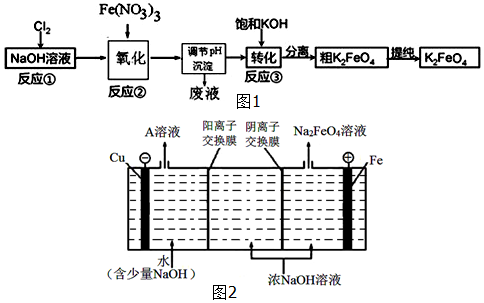
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com