
| A. | ①②③④ | B. | ②③④ | C. | ①②③ | D. | ③④ |
分析 ①同温同压下,密度之比等于摩尔质量之比;
②根据n=$\frac{m}{M}$知道质量相同时物质的量之比与摩尔质量成反比,H2、D2、T2分子都含有2个质子,据此判断;
③结合H2、D2、T2分子含有中子数判断;
④同温同压下,体积之比等于物质的量之比.
解答 解:①同温同压下,密度之比等于摩尔质量之比,故H2、D2、T2三种气体的摩尔质量之比=2g/L:4g/mol:6g/mol=1:2:3,故①正确;
②根据n=$\frac{m}{M}$可知,相同质量时,物质的量之比与摩尔质量成反比,等质量H2、D2、T2三种气体的物质的量之比=6g/mol:4g/mol:2g/mol=6:3:2,H2、D2、T2分子都含有2个质子,故质子数之比=气体物质的量之比=6:3:2,故②正确;
③等质量H2、D2、T2三种气体的物质的量之比为6:3:2,H2、D2、T2分子分别含有中子数为0、2、4,故中子数之比=0:6:8=0:3:4,故③正确;
④等质量H2、D2、T2三种气体的物质的量之比为6:3:2,同温同压下,体积之比等于物质的量之比=6:3:2,故④正确,
故选A.
点评 本题考查物质的量相关计算,难度不大,注意对公式的理解与灵活应用.


科目:高中化学 来源: 题型:选择题
| A. | Si 1s22s22p2 | B. | O2- 1s22s22p6 | ||
| C. | Na+ 1s22s22p6 | D. | Al 1s22s22p63s23p1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| T | M层电子数比K层电子数多4个 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
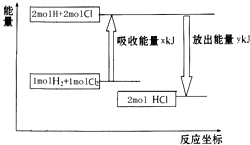
| A. | 该反应是放热反应 | |
| B. | 断裂1 mol H-H键和1 mol Cl-Cl 键放出x kJ能量 | |
| C. | 断裂1 mol H-Cl键需要吸收y kJ的能量 | |
| D. | 2 mol HCl的总能量高于1 mol H2和1 molCl2的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相 关 信 息 |
| R | R在周期表中的周期数、族序数与其原子序数均相等 |
| X | X原子形成的化合物种类最多 |
| Y | Y的氢化物与其最高价氧化物的水化物化合生成一种盐 |
| Z | Z原子的最外层电子数为K层电子数的3倍 |
| Q | Q存在质量数为23,中子数为12的核素 |
| w | W在所处周期中原子半径最小 |
 .R、X、Z可以形成X2R6Z2化合物,1mol该物质与足量的金属钠反应生成1mol氢气,则该物质的结构简式是CH2OHCH2OH,请写出该物质的一种主要用途汽车发动机的抗冻剂.
.R、X、Z可以形成X2R6Z2化合物,1mol该物质与足量的金属钠反应生成1mol氢气,则该物质的结构简式是CH2OHCH2OH,请写出该物质的一种主要用途汽车发动机的抗冻剂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
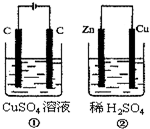 如图所示的两个实验装置中,溶液的体积均 为200mL,开始时电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得导线中均通过0.01mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中不正确的是( )
如图所示的两个实验装置中,溶液的体积均 为200mL,开始时电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得导线中均通过0.01mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中不正确的是( )| A. | 右边电极上生成物质的物质的量:①=② | |
| B. | 相同状态下电极上产生气体的体积:①=② | |
| C. | 溶液的pH变化:①减小,②增大 | |
| D. | 电极反应式①中阴极Cu2++2e-═Cu:②中负极:Zn-2e-═Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 纤维素在稀硫酸、加热的条件下水解 | |
| B. | 棉制品吸湿性好和分子中具有-OH有关 | |
| C. | 纤维指的就是纤维素 | |
| D. | 纤维素因分子结构中含-OH,可和浓HNO3发生硝化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当一个化学反应达到一定反应限度时,该反应就停止了 | |
| B. | 化学反应速率为“0.8mol•L-1•s-1”表示的意思是:时间为1s时,某物质的浓度为0.8mol•L-1 | |
| C. | 根据化学反应速率的大小可以知道化学反应进行的限度 | |
| D. | 对于不同的化学反应而言,化学反应速率大的不一定反应就快 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com