
一定温度下,在2L密闭容器中发生下列反应:4NO2(g)+O2(g)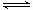 2N2O5(g);已知该反应的平衡常数:
2N2O5(g);已知该反应的平衡常数: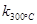 >
>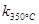 ,且体系中
,且体系中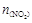 (单位:mol)随时间变化如下表:
(单位:mol)随时间变化如下表:
|
时间(s) |
0 |
500 |
1000 |
1500 |
|
t1℃ |
20 |
13.96 |
10.08 |
10.08 |
|
t2℃ |
20 |
a |
b |
c |
下列说法一定正确的是( )
A.正反应为吸热反应
B.如果t2℃<t1℃,那么 a>b=c,且a=10+0.5b
C.如果t2℃<t1℃,那么t2℃达到平衡的时间介于1000s至1500s之间
D.如果t2℃>t1℃,那么b>10.08
D
【解析】
试题分析:A.该反应的平衡常数:k300℃>k350℃,温度越大,平衡常数越小,即升高温度,平衡逆向移动,所以正反应为放热反应,故A错误;B.如果t2℃<t1℃,t1℃反应快,先达到平衡,但b与c也不一定相等,而且20-a>a-b,所以a>10+0.5b,故B错误;C.如果t2℃<t1℃,那么t2℃达到平衡的时间应该在t1℃后,但是t1℃达到平衡的时间可能是小于1000s,那么t2℃达到平衡的时间也就不能确定了,故C错误;D.如果t2℃>t1℃,那么t2℃时反应较快,1000s时已经达到了平衡,而且升温时平衡向左移动,n(NO2)>10.8,故D正确;
考点:考查可逆反应在不同温度下达到平衡时各物质的浓度与时间及反应放出或吸收热量的关系的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
一定温度下,l mol X和n mol Y在体积为2L的密 闭容器中发生如下反应:( )
X(g)+Y(g)![]() 2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
A.用X表示此反应的反应速率是(0.1—0.2a)mol·(L·min)-1
B.当混合气体的质量不再发生变化时,说明反应达到平衡状态
C.向平衡后的体系中加入l mol M,平衡向逆反应方向移动
D.向上述平衡体系中再充入l mol X,v(正)增大,v(逆)减小,平衡正向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com