
【题目】下列各组混合物中上下分层的是( )
A.乙酸和乙醇B.酒精和水
C.乙酸乙酯和水D.溴和苯
 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
【题目】汽车内燃机工作时会引起N2和O2的反应:N2+O2![]() 2NO,是导致汽车尾气中含有NO的原因之一。
2NO,是导致汽车尾气中含有NO的原因之一。
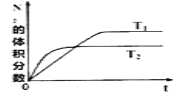
(1)在T1、T2温度下,一定量的NO(g)发生分解反应时,N2的体积分数随时间变化如图所示,根据图像判断反应N2(g)+O2(g)![]() 2NO(g)的△H_____0(填“>"或“<”)。
2NO(g)的△H_____0(填“>"或“<”)。
(2)在T3温度下,向2L密闭容器中充入10molN2与5molO2,50秒后达到平衡,测得NO的物质的量为2mol,则该反应的速率v(N2)=_________。该温度下,若增大压强此反应的平衡常数将_________(填“增大”、“减小”、“不变”或“无法确定”),若向上述容器中再充入2molN2(g)与1molO2(g),则再次达到平衡时O2的转化率________(填“增大”、“减小”、“不变”或“无法确定”)。
(3)研究发现,用CH4催化还原NOx可以消除氮氧化物的污染,从而达到脱硝的目的:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJmol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJmol-1
甲烷直接被NO2还原为N2的热化学方程式为______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】11.2 g铁粉与2.2 g硫粉均匀混合,在密闭容器中加热,冷却后加入足量盐酸,在标准状况下收集到气体的体积是( )
A. 11.2 L B. 5.6 L C. 4.48 L D. 2.24 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,二元弱酸H2A溶液中滴加NaOH溶液,所得混合溶液pH与离子浓度变化如图所示,下列说法正确的是( )

A. 直线M表示pH与lg![]() 的变化关系
的变化关系
B. Ka2(H2A)=10-4.3
C. 交点e的溶液中:c(H2A)=c(A2-)>c(HA-)>c(H+)>c(OH-)
D. f点溶液中:c(H+)-c(OH-)=c(HA-)+c(A2-)-c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响,在室温下按照如下方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10mL2% H2O2溶液 | 无 |
② | 10mL5% H2O2溶液 | 无 |
③ | 10mL5% H2O2溶液 | 1mL0.1mol/LlFeCl3溶液 |
④ | 10mL5% H2O2溶液+少量HCI溶液 | 1mL0.1mol/LlFeCl3溶液 |
⑤ | 10mL5%H2O2溶液+少量NaOH溶液 | 1mL0.1mol/LlFeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是__________________________。
(2)实验①和②的目的是_________________________。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进________________________。
(3)写出实验③的化学反应方程式___________________________________。
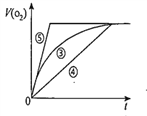
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。分析上图能够得出的实验结论是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7是一种重要的化工原料。以铬铁矿(主要成分为FeO·Cr2O3,还含有Al2O3、Fe2O3等杂质)为原料制备K2Cr2O7的一种工艺流程如下:

已知:
①4FeO·Cr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
②Cr2O72-+H2O![]() 2CrO42-+2H+
2CrO42-+2H+
(1)“焙烧”时,Al2O3与Na2CO3发生反应的化学方程式为___________。
(2)“滤渣”的主要成分是________(填化学式).
(3)“酸化”步骤调节溶液pH<5,其目的是_________
(4)“转化”一步发生反应的化学方程式为____________
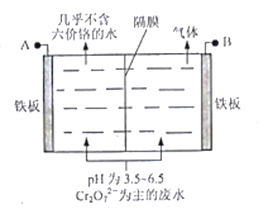
(5)采用电解法处理含铬废水原理如下图所示。阳极区溶液中发生反应:Cr2O72-+6Fe2++14H+ == 2Cr3+ +6Fe3+ + 7H2O,阳极的电极反应式为_______,阴极产生的气体为_______(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com