
某学习小组进行了下图所示的实验,实验后组员之间的交流不合理的是

A.甲同学认为试管b中收集到的气体可点燃,且产生淡蓝色 火焰
B.乙同学认为试管a中生成的黑色固体可能为四氧化三铁
C.丙同学认为可用盐酸和KSCN溶液来验证产物中的三价铁
D.丁同学认为将少量还原性铁粉放入试管中,加适量的水,加热也可实现该反应
科目:高中化学 来源:2014-2015内蒙古北方重工业集团三中高一下学期第一次月考化学试卷(解析版) 题型:选择题
已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是
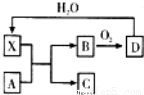
A.X使蔗糖变黑的现象主要体现了X的强氧化性
B.若A为铁,则足量A与X在室温下即可完全反应
C.若A为碳单质,则将C通入少量的澄清石灰水中,一定可以观察到有白色沉淀产生
D.工业上,B转化为D的反应条件为高温、常压、使用催化剂
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:填空题
(12分)有机物键线式结构的特点是以线示键,每个折点和线端处表示有一个碳原子,并以氢补足四键,C、H不表示出来,其它原子或原子团要表示出来,例如:CH3CHOHCH3的键线式结构为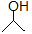 。CH3CH=CHCH3是石油裂解的产物之一,它的键线式结构可表示为
。CH3CH=CHCH3是石油裂解的产物之一,它的键线式结构可表示为 。
。
(1)CH3CH=CHCH3的名称为 ,其所含官能团的结构式为 ,与H2在一定条件下发生加成反应,其产物的同分异构体的键线式结构为 。
(2)完成下列反应方程式,产物用键线式表示: +Br2→ ,反应类型为 反应。
+Br2→ ,反应类型为 反应。
(3) 是一种加聚产物,则其单体的结构简式为 ,其链节为 。
是一种加聚产物,则其单体的结构简式为 ,其链节为 。
(4)写出与CH3CH=CHCH3含有相同官能团的同分异构体的结构简式 。(任写一种)
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北宜昌市高二3月月考化学试卷(解析版) 题型:选择题
下列过程中,共价键被破坏的是
A.碘升华 B.溴溶于CCl4 C.蔗糖溶于水 D.HCl溶于水
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省高一3月月考化学试卷(解析版) 题型:选择题
工业上可利用反应2NaClO3 + SO2 + H2SO4= 2ClO2 + 2NaHSO4来制取ClO2,下列关于该反应的说法正确的是
A.SO2发生还原反应 B.NaClO3失去电子
C.H2SO4作氧化剂 D.1mol氧化剂得到1mol电子
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省襄阳市高二3月月考化学试卷(解析版) 题型:填空题
(14分)红磷P(s)和Cl2 (g)发生反应生成PCl3(g)和 PCl5(g),反应过程如下。
2P(s) + 3Cl2(g) = 2PCl3(g) △H=-612kJ/mol
2P(s) + 5Cl2(g) = 2PCl5(g) △H=-798kJ/mol
请回答下列问题。
(1)气态 PCl5生成气态PCl3和Cl2的热化学方程式为 。
(2)PC15生成 PCl3和Cl2是一个可逆反应,向5.0L密闭容器中充入0.1 md PCl5(g),反应在不同条件下进行,反应体系总压强随时间的变化关系如图所示。
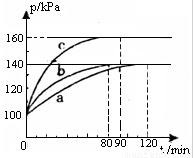
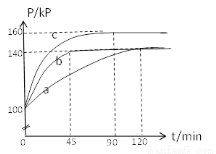
①实验b中PCl5的平衡分解率为 ,其他条件不变,在该实验中再加入 0.1 mol PCl5 (g) ,平衡分解率 (填“增大”、“减小”或“不变”)。
②与实验a相比,c改变的条件是 ,判断依据是 。
(3)PCl5露置于潮湿空气中,能水解生成两种中学化学常见酸,其化学方程式为 。
(4)人的牙齿表面有一层釉质,其组成为羟基磷灰石 Ca5( PO4)3OH(Ksp=6.8×10-37)。为了防止蛀牙,人们常使用含氟离子的牙膏,其中的氟化物可使轻基磷灰石转化为氟磷灰石Ca5( PO4)3F(Ksp=1.0×10-60)。写出该反应的离子方程式 ,该反应的平衡常数为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省襄阳市高二3月月考化学试卷(解析版) 题型:选择题
下列叙述中,正确的是
A.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子
B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子
C.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高
D.某基态原子错误的核外电子排布图为 该排布图违背了泡利原理
该排布图违背了泡利原理
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省高三下学期第一次模考化学试卷(解析版) 题型:填空题
(14分)
(1)已知:①N2(g)+O2(g)=2NO(g) △H=+179.5 kJ/mol
②2NO(g)+O2(g)=2NO2(g) △H=-112.3 kJ/mol
③2NO(g)+2CO(g)=N2(g) +2CO2(g) △H=-759.8 kJ/mol
NO2(g)+CO(g)=NO(g) +CO2(g) △H= kJ/mol。
(2)将不同物质的量的H2O(g)和CO(g)分别通入体积为2 L的恒容密闭容器中,进行反应:H2O(g)+CO(g)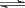 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min[ | ||
H2O | CO | CO | H2 | |||
① | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
② | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
③ | 900 | a | b | c | d | t |
①实验组①中以v(CO2)表示的反应速率为 ,此温度下的平衡常数为 ,温度升高时平衡常数会 (填“增大”、“减小”或“不变”)。
②650 ℃时,若在此容器中开始充入2 mol H2O(g)、 1 mol CO、 1 mol CO2和 2 mol H2,若要使反应在开始时 进行。(填“正向”、“逆向”)
③若a=2,b=1,则c= ,达平衡时实验组②中H2O(g)和实验组③中CO的转化率的关系为
α2 (H2O) α3 (CO)(填“<”、“>”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com