
ijŅ©Īļ±ūæÉÓÉÓŠ»śĪļ¼×ŗĶŅŅŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦ÖʵĆ
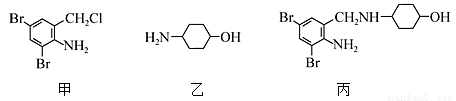
ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ
A£®¼×”¢ŅŅŗĶ±ū¶¼ŹōÓŚ·¼Ļć×å»ÆŗĻĪļ B£®ŅŅÄÜÓėŃĪĖį·“Ó¦µ«²»ÄÜÓėNaOHČÜŅŗ·“Ó¦
C£®±ūŹĒÓɼ×ŗĶŅŅĶعż¼Ó³É·“Ó¦ÖĘµĆµÄ D£®±ūÖŠµÄĮ½øöĮłŌŖ»·ÉĻµÄĢ¼Ō×ÓÓŠæÉÄܹ²Ę½Ćę

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016ğȫ¹śĘÕĶØøßµČѧŠ£ÕŠÉśĶ³Ņ»æ¼ŹŌ»Æѧ£ØČ«¹ś1¾ķ²Īæ¼°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżÖµ”£ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ
A£®14 gŅŅĻ©ŗĶ±ūĻ©»ģŗĻĘųĢåÖŠµÄĒāŌ×ÓŹżĪŖ2NA
B£®1 molN2Óė4 mol H2·“Ӧɜ³ÉµÄNH3·Ö×ÓŹżĪŖ2NA
C£®1 molFeČÜÓŚ¹żĮæĻõĖį£¬µē×Ó×ŖŅĘŹżĪŖ2NA
D£®±ź×¼×“æöĻĀ£¬2.24 LCCl4ŗ¬ÓŠµÄ¹²¼Ū¼üŹżĪŖ0.4NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğÕć½Ź”ĪĀÖŻŹŠŹ®Š£ĮŖŗĻø߶žĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ijĶ¬Ń§Éč¼ĘĮĖÓÉŅŅ“¼ŗĻ³ÉŅŅ¶ž“¼µÄĀ·ĻßČēĻĀ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
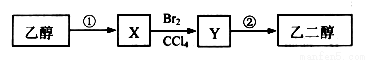
A. XæÉŅŌ·¢Éś¼Ó³É·“Ó¦
B. µČĪļÖŹµÄĮæµÄŅŅ“¼”¢XĶźČ«Č¼ÉÕ£¬ĻūŗÄŃõĘųµÄĮæ²»ĻąĶ¬
C. ²½Öč¢ŚŠčŅŖŌŚĒāŃõ»ÆÄĘ“¼ČÜŅŗÖŠ·“Ó¦
D. ²½Öč¢ŁµÄ·“Ó¦ĄąŠĶŹĒĖ®½ā·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğÕć½Ź”ĪĀÖŻŹŠŹ®Š£ĮŖŗĻø߶žĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹Ų»ÆѧŹ·ŗĶ»Æѧъ¾æ·½·ØµÄŠšŹöÖŠÕżČ·µÄŹĒ£Ø £©
¢ŁĪŅ¹śæĘѧ¼ŅŌŚŹĄ½ēÉĻµŚŅ»“ĪČĖ¹¤ŗĻ³É½į¾§Å£ŅȵŗĖŲ£¬½ŅæŖĮĖČĖ¹¤ŗĻ³ÉÓŠ»śĪļ“ó·Ö×ÓµÄæŖ¶Ė£»¢ŚĄī±ČĻ£Ģį³öĮĖĄūÓĆŃõ»ÆĶŌŚøßĪĀĻĀŃõ»ÆÓŠ»śĪļÉś³ÉCO2”¢H2OĄ“Č·¶ØÓŠ»śĪļµÄŌŖĖŲ×é³É£»¢ŪĆĄ¹ś»Æѧ¼ŅæĘĄļ““Į¢ĮĖÓŠ»ś»ÆѧµÄ”°ÄęŗĻ³É·ÖĪöĄķĀŪ”±ĪŖÓŠ»śŗĻ³É·ÖĪöÖøĆ÷ĮĖĖ¼æ¼µÄ·½Ļņ£»¢Ü ÄĘČŚ·Øæɶ؊ŌČ·¶ØÓŠ»śĪļÖŠŹĒ·ńŗ¬ÓŠµŖ”¢ĀČ”¢ä唢Įņ£»¢Ż1828ÄźĪ¬ĄÕŹ×ĻČŌŚŹµŃéŹŅŗĻ³ÉÄņĖŲ£¬æŖ““ĮĖĪŽ»śĪļŗĻ³ÉÓŠ»śĪļµÄĄśŹ·”£
A£®Ö»ÓŠ¢Ł B£®¢ŁŗĶ¢Ū C£®¢Ł¢Ū¢Ż D£®¢Ł¢Ś¢Ū¢Ü¢Ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğÕć½Ź”ø߶žĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚ½ųŠŠÓŠ¹ŲĪļÖŹŠŌÖŹµÄĢ½¾æŹµŃ鏱£¬ĻĀĮŠŹµŃéÄܹ»“ļµ½ŹµŃéÄæµÄµÄŹĒ
A£®½«æķ¶Č0.2”«0.3cmµÄĀĮĢõŌŚ¾Ę¾«µĘ»šŃęÉĻ×ĘÉÕʬæĢ£¬æɹŪ²ģµ½ĀĮĢõĀķÉĻ¾ēĮŅČ¼ÉÕ
B£®ĪŖĮĖÅąŃų“óæÅĮ£µÄĆ÷·Æ¾§Ģ壬ÅäÖĘ90”ęµÄ±„ŗĶČÜŅŗŗóÖčĄä
C£®×öŅŅ“¼170”ꏱµÄĶŃĖ®ŹµŃéÖĘČ”ŅŅĻ©Ź±£¬ĪŖŹ¹ÉÕĘæŹÜČČ¾łŌČ£¬ĪĀ¶ČĀżĀżÉĻÉżµ½170”ę
D£®ĪŖĮĖ¼ģŃéij¹¤Ņµ·ĻĖ®ÖŠµÄ·ÓĄąĪļÖŹŹĒ·ń“ęŌŚ£¬ÓĆČżĀČ»ÆĢśČÜŅŗ¼ģŃé
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğÕć½Ź”ø߶žĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®9.2æĖ¼×±½ŗ¬ÓŠµÄC£HŹżÄæĪŖ0.8NA
B£®1 molōĒ»łĖłŗ¬µÄµē×ÓŹżĪŖ7NA
C£®1 molŅŅ“¼“ß»ÆŃõ»ÆÉś³ÉŅŅČ©Ź±×ŖŅʵĵē×ÓŹżĪŖ4NA
D£®·Ö×ÓŹ½ĪŖC3H6µÄÓŠ»śĪļŅ»¶Øŗ¬ÓŠNAøöĢ¼Ģ¼Ė«¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģŗÓÄĻŹ”ŌĶĘ¼öøßČżĖÄŌĀøßæ¼·ĀÕęÄ£ÄāĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ¼ņ“šĢā
”¾»Æѧ”Ŗ”ŖŃ”ŠŽ3£ŗĪļÖŹ½į¹¹ÓėŠŌÖŹ”æ
ĪļÖŹµÄ½į¹¹¾ö¶ØĪļÖŹµÄŠŌÖŹ”£Ēė»Ų“šĻĀĮŠÉę¼°ĪļÖŹ½į¹¹ŗĶŠŌÖŹµÄĪŹĢā£ŗ
£Ø1£©µŚ¶žÖÜĘŚÖŠ£¬ŌŖĖŲµÄµŚŅ»µēĄėÄÜ“¦ÓŚBÓėNÖ®¼äµÄŌŖĖŲÓŠ_________ÖÖ”£
£Ø2£©Ä³ŌŖĖŲĪ»ÓŚµŚĖÄÖÜĘŚ¢ų×壬Ę仳Ģ¬Ō×ÓµÄĪ“³É¶Ōµē×ÓŹżÓė»łĢ¬Ģ¼Ō×ÓµÄĪ“³É¶Ōµē×ÓŹżĻąĶ¬£¬ŌņĘ仳Ģ¬Ō×ӵļŪ²ćµē×ÓÅŲ¼Ź½ĪŖ_________________”£
£Ø3£©ŅŅĻ©ĶŖ£ØCH2£½C£½O£©ŹĒŅ»ÖÖÖŲŅŖµÄÓŠ»śÖŠ¼äĢ壬æÉÓĆCH3COOHŌŚ£ØC2H5O£©3P£½O“ęŌŚĻĀ¼ÓČČĶŃH2OµĆµ½”£ŅŅĻ©ĶŖ·Ö×ÓÖŠĢ¼Ō×ÓŌӻƹģµĄĄąŠĶŹĒ_____________£¬1mol£ØC2H5O£©3P£½O·Ö×ÓÖŠŗ¬ÓŠµÄ¦Ņ¼üµÄŹżÄæĪŖ__________________”£
£Ø4£©ŅŃÖŖ¹ĢĢ¬NH3”¢H2O”¢HFµÄĒā¼ü¼üÄÜŗĶ½į¹¹ČēĻĀ£ŗ
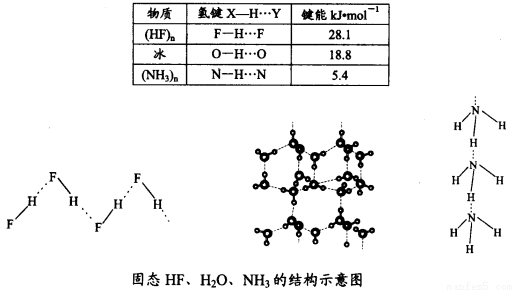
½āŹĶH2O”¢HF”¢NH3·ŠµćŅĄ“Ī½µµĶµÄŌŅņ___________________”£
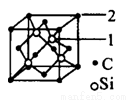
£Ø5£©Ģ¼»Æ¹čµÄ½į¹¹Óė½šøÕŹÆĄąĖĘ£¬ĘäÓ²¶Č½ö“ĪÓŚ½šøÕŹÆ£¬¾ßÓŠ½ĻĒæµÄÄĶÄ„ŠŌÄÜ”£Ģ¼»Æ¹č¾§°ū½į¹¹ÖŠĆæøöĢ¼Ō×ÓÖÜĪ§ÓėĘä¾ąĄė×ī½üµÄ¹čŌ×ÓÓŠ___________øö£¬ÓėĢ¼Ō×ÓµČ¾ąĄė×ī½üµÄĢ¼Ō×ÓÓŠ__________øö”£ŅŃÖŖĢ¼»Æ¹č¾§°ū±ß³¤ĪŖapm£¬Ōņ¾§°ūĶ¼ÖŠ1ŗŹčŌ×ÓŗĶ2ŗÅĢ¼Ō×ÓÖ®¼äµÄ¾ąĄėĪŖ________pm£¬Ģ¼»Æ¹čµÄĆܶČĪŖ__________g£Æcm3”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģ¹ć¶«Ź”·šÉ½ŹŠøßČż4ŌĀ¶žÄ£Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
¼ŗ¶žĖįŹĒŗĻ³ÉÄįĮś£66µÄÖ÷ŅŖŌĮĻÖ®Ņ»”£ŹµŃéŹŅŗĻ³É¼ŗ¶žĖįµÄŌĄķ”¢ÓŠ¹ŲŹż¾Ż¼°×°ÖĆŹ¾ŅāĶ¼ČēĻĀ£ŗ3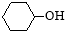 £«8HNO3 ”Ŗ”ś 3
£«8HNO3 ”Ŗ”ś 3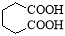 £«8NO”ü£«7H2O
£«8NO”ü£«7H2O

ŹµŃé²½ÖčČēĻĀ£ŗ
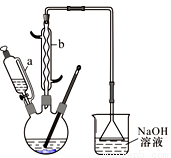
¢ń£®ŌŚČżæŚÉÕĘæÖŠ¼ÓČė16 mL 50%µÄĻõĖį£ØĆܶČĪŖ1.31 g/cm3£©£¬ŌŁ¼ÓČė1”«2Į£·ŠŹÆ£¬µĪŅŗĀ©¶·ÖŠŹ¢·ÅÓŠ5.4 mL»·¼ŗ“¼”£
¢ņ£®Ė®Ō”¼ÓČČČżæŚÉÕĘæÖĮ50”ę×óÓŅ£¬ŅĘČ„Ė®Ō”£¬»ŗĀżµĪ¼Ó5”«6µĪ»·¼ŗ“¼£¬Ņ”¶ÆČżæŚÉÕĘ棬¹Ū²ģµ½ÓŠŗģ×ŲÉ«ĘųĢå·Å³öŹ±ŌŁĀżĀżµĪ¼ÓŹ£ĻĀµÄ»·¼ŗ“¼£¬Ī¬³Ö·“Ó¦ĪĀ¶ČŌŚ60 ”ꔫ65 ”ęÖ®¼ä”£
¢ó£®µ±»·¼ŗ“¼Č«²æ¼ÓČėŗ󣬽«»ģŗĻĪļÓĆ80 ”ꔫ90 ”ęĖ®Ō”¼ÓČČŌ¼10 min£Ø×¢ŅāæŲÖĘĪĀ¶Č£©£¬Ö±ÖĮĪŽŗģ×ŲÉ«ĘųĢåÉś³ÉĪŖÖ¹”£
¢ō£®³ĆČČ½«·“Ó¦Ņŗµ¹ČėÉÕ±ÖŠ£¬·ÅČė±łĖ®Ō”ÖŠĄäČ“£¬Īö³ö¾§Ģåŗó¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ”¢³ĘÖŲ”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©×°ÖĆbµÄĆū³ĘĪŖ £¬Ź¹ÓĆŹ±ŅŖ“Ó £ØĢī”°ÉĻæŚ”±»ņ”°ĻĀæŚ”±£©ĶØČėĄäĖ®£»µĪŅŗĀ©¶·µÄĻøÖ§¹ÜaµÄ×÷ÓĆŹĒ
£Ø2£©±¾ŹµŃéĖłÓĆ50£„µÄĻõĖįµÄĪļÖŹµÄĮæÅضČĪŖ £»ŹµŃéÖŠ£¬µŖŃõ»ÆĪļ·Ļ
Ęų£ØÖ÷ŅŖ³É·ÖĪŖN02ŗĶNO)æÉŅŌÓĆNaOHČÜŅŗĄ“ĪüŹÕ£¬ĘäÖ÷ŅŖ·“Ó¦ĪŖ£ŗ
2N02+2NaOH=NaN02+NaN03+H20ŗĶNO+N02+2NaOH=2NaN02+H20
ĘäÖŠNaOHČÜŅŗæÉŅŌÓĆNa2C03ČÜŅŗĄ“Ģę“ś£¬ĒėÄ£·ĀÉĻŹö·“Ó¦£¬Š“³öNa2C03ČÜŅŗĪüŹÕµÄĮ½øö·½³ĢŹ½£ŗ
£»
£Ø3£©ĻņČżæŚÉÕĘæÖŠµĪ¼Ó»·¼ŗ“¼Ź±£¬·“Ó¦ĪĀ¶ČŃøĖŁÉĻÉż£¬ĪŖŹ¹·“Ó¦ĪĀ¶Č²»ÖĀ¹żøߣ¬±ŲŅŖŹ±æɲÉČ”µÄ“ėŹ©ŹĒ ”£
£Ø4£©ĪŖĮĖ³żČ„æÉÄܵÄŌÓÖŹŗĶ¼õÉŁ²śĘ·ĖšŹ§£¬æÉ·Ö±šÓĆ ŗĶ Ļ“µÓ¾§Ģ唣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĮÉÄžŹ”øßŅ»ĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚŅ»¶ØĪĀ¶ČĻĀµÄ¶ØČŻĆܱÕČŻĘ÷ÖŠ£¬µ±ĪļÖŹµÄĻĀĮŠĪļĄķĮæ²»ŌŁ±ä»ÆŹ±£¬²»ÄÜĖµĆ÷·“Ó¦A(s)£«2B(g) C(g)£«D(g)ŅŃ“ļĘ½ŗāדĢ¬µÄŹĒ
C(g)£«D(g)ŅŃ“ļĘ½ŗāדĢ¬µÄŹĒ
A£®»ģŗĻĘųĢåµÄŃ¹Ēæ B£®»ģŗĻĘųĢåµÄĆܶČ
C£®BµÄĪļÖŹµÄĮæÅØ¶Č D£®ĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com