
按下图所示装置进行实验,并回答下列问题: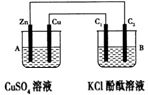
(1)判断装置的名称:A池为 ,B池为 。
(2)锌极为 极,电极反应式为 ;铜极为 极,电极反应式为 ;石墨棒C1为 极,电极反应式为 ;石墨棒C2附近发生的实验现象为 ,反应结束后,B池溶液的pH值 。(增大、减小、不变,忽略气体溶于水) 。
(3)当C2极析出224 mL气体(标准状况下),锌的质量 (增加或减少) g。
(1)原电池(1分) 电解池(1分)
(2)负极(1分)Zn-2e-=Zn2+ (2分)正极(1分)Cu2++2e-="Cu" (2分)
阳极(1分) 2Cl--2e-=Cl2↑,(2分) 有气体生成,溶液变红(2分) 增大(1分)
(3)减少 (1分) 0.65(1分)
解析试题分析:(1)锌与硫酸铜可以发生自发的氧化还原反应,因此A装置是原电池。B装置中电极均是惰性电极,属于电解池。
(2)原电池中较活泼的金属作负极,则锌是负极失去电子,发生氧化反应,电极反应式为Zn-2e-=Zn2+;银是正极,溶液中的铜离子在正极得到电子发生还原反应,电极反应式为Cu2++2e-=Cu。C1电极与原电池的正极相连作阳极,溶液中的氯离子放电,电极反应式为2Cl--2e-=Cl2↑。C2电极与原电池的负极相连作阴极,溶液中的氢离子放电,电极反应式为2H++2e-=H2↑。由于氢离子放电破坏阴极周围水的电离平衡,导致阴极周围氢离子浓度小于氢氧根离子浓度,溶液显碱性,碱能使酚酞显红色。B装置中总的化学方程式为2KCl+2H2O 2KOH+H2↑+Cl2↑,即装置中有氢氧化钾强碱生成,因此溶液的碱性增强。
2KOH+H2↑+Cl2↑,即装置中有氢氧化钾强碱生成,因此溶液的碱性增强。
(3)若工作一段时间后,生成标准状况下氢气224ml,其物质的量是0.01mol,转移电子的物质的量是0.02mol。根据电子转移守恒可知消耗锌的物质的量是0.01mol,质量减少0.01mol×65g/mol=0.65g。
考点:考查电化学原理的应用


科目:高中化学 来源: 题型:填空题
(每空1分,共8分)
利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池。请填写下列空白:
(1)实验原理:Fe+2H+ Fe2++H2↑。
Fe2++H2↑。
(2)实验用品:电极( 、 )、稀硫酸、 (填写所缺的实验用品)、耳机(或者电流计)。
(3)实验装置:
(4)原电池设计及注意的问题。
①按如图所示连接好实验仪器,注意观察(耳朵听)耳机是否有声音发出,如果没有,可将原电池的两个电极中的一极接触耳机插头上的一极(注意:接触的同时耳机的另一个极是连接在原电池的另一个电极上的),这时可以听见耳机发出“嚓嚓嚓”声音。其原因是:在原电池中,由化学能转化为 。
②如果将装置中的耳机改为电流计,则铁钉应该接电流计的 极,电极反应是 ;另一极应该接电流计的 极,电极发生了 反应(“氧化”或“还原”)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(9分)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiCIO4。溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。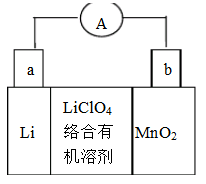
回答下列问题:
(1)外电路的电流方向是由____极流向____极。(填字母)
(2)电池正极反应式为____。
(3)是否可用水代替电池中的混合有机溶剂?____(填“是”或“否”),原因是____________。
(4)MnO2可与KOH和KClO3,在高温下反应,生成K2MnO4,反应的化学方程式为_______________。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(9分)
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为 、 。
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是 ,电解氯化钠溶液的总反应方程式为 ;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为
(法拉第常数F=9.65×l04C.mol-1,列式计算),最多能产生的氯气体积为 L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图所示的装置中电极a、b均为碳棒,两烧杯中所盛溶液均为500mL1.0mol/L。
⑴A为 (填“原电池”或“电解池”),其中Ag电极的电极反应式为: ;发生 反应(填“氧化”或“还原”)。
⑵B装置中的电极b极为 极,电极反应式为 ,
总反应的化学方程式为 。
⑶工作一段时间后,当Zn片质量减少6.5g时,a极逸出的气体在标准状况下的体积 L。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在一个U形管里盛有CuCl2溶液,并插入两块锌片作电极,按如图连接。
(1)如果把电键K接A,该装置应是电解装置,Zn①极是 极,电极反应式为 ,Zn②极是 极,电极反应式为 。
(2)上述反应进行5 min后,转换电键K到C,则这个装置是原电池装置,Zn①极是 极,电极反应式为 。
(3)上述装置进行2 min后,再转换电键K到B,则Zn①极发生的化学反应为 ,Zn②极发生的有关电化学的反应为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氧化钠辖液电解实验,如图所示。
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为 、 。[来源:学科网ZXXK]
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是 ,电解氯化钠溶液的总反应方程式为 ;
(3)若每个电池甲烷通如量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为 (法拉第常数F=9.65×l04C · mol-1列式计算),最多能产生的氯气体积为 L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
可以将氧化还原反应2H2+O2 2H2O设计成原电池。
2H2O设计成原电池。
(1)利用氢气和氧气、氢氧化钾溶液构成燃料电池,则负极通的气体应是 ,正极通的气体就是 ,电极反应为:正极 ,负极 。
(2)如果把KOH改为稀硫酸作电解质,则电极反应为:正极: ,负极: 。
(3)(1)和(2)的电解质溶液不同,反应进行后,其溶液的pH各有何变化? 。
(4)如把H2改为甲烷,KOH溶液作电解质溶液,则电极反应为:正极: ,负极: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
甲、乙的实验装置如图所示,丙、丁分别是氯碱工业生产示意图和制备金属钛的示意图。
请回答下列问题:
(1)写出甲装置中碳棒表面的电极反应式:_________________________
(2)已知:5Cl2+I2+6H2O=10HCl+2HIO3。若将湿润的淀粉KI试纸置于乙装置中的碳棒附近,现象为________________________________;若乙装置中转移0.02 mol电子后停止实验,烧杯中溶液的体积为200 mL,则此时溶液的pH=________。(室温条件下,且不考虑电解产物的相互反应)
(3)工业上经常用到离子交换膜,离子交换膜有阳离子交换膜和阴离子交换膜两种,阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过。当乙装置中的反应用于工业生产时,为了阻止两极产物之间的反应,通常用如丙图所示的装置,Na+的移动方向如图中标注,则H2的出口是________(填“C”、“D”、“E”或“F”);________(填“能”或“不能”)将阳离子交换膜换成阴离子交换膜。
(4)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaO作电解质,利用丁装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。
①写出阳极的电极反应式:_____________________________________。
②在制备金属钛前后,CaO的总量不变,其原因是(请结合化学用语解释)____________________________________ __。
③电解过程中需定期更换阳极材料的原因是
___________________ __________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com