

| A. | 锌做负极发生氧化反应 | |
| B. | 供电时的总反应为:Zn+2H+═Zn2++H2↑ | |
| C. | 该装置可实现化学能转化为电能 | |
| D. | 产生1 g H2,消耗锌的质量65 g |
分析 锌比铜活泼,锌为负极,发生氧化反应,铜为正极,发生还原反应,原电池工作时总反应为:Zn+H+=Zn2++H2↑,原电池是化学能转化为电能的装置,以此解答该题.
解答 解:A.锌为负极,Zn失电子发生氧化反应,故A正确;
B.原电池工作时总反应为:Zn+2H+=Zn2++H2↑,故B正确;
C.该装置为原电池,原电池是化学能转化为电能的装置,故C正确;
D.原电池工作时总反应为:Zn+2H+=Zn2++H2↑,产生1molH2,消耗锌的质量65g,故D错误;
故选D.
点评 本题考查原电池知识,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,有利于培养学生的良好的科学素养,提高学习的积极性,难度不大,注意把握原电池的工作原理.


科目:高中化学 来源: 题型:选择题
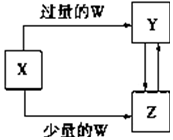 已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是( )
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是( )| 选项 | W | X |
| A | 稀硫酸 | NaAlO2溶液 |
| B | 稀硝酸 | Fe |
| C | CO2 | Ca(OH)2溶液 |
| D | Cl2 | Fe |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
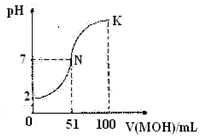
| A. | 在N到K间任意一点对应的溶液中:c(M+)+c(H+)=c(OHˉ)+c(Aˉ) | |
| B. | HA为弱酸 | |
| C. | 常温下,MA溶液的pH>7 | |
| D. | N点水的电离程度小于K点水的电离程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| X | |||
| W |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 我们的祖先很早就学会了烧制陶瓷、冶炼金属、酿造酒类 | |
| B. | 化学研究的主要目的是认识分子 | |
| C. | 化学科学无法帮助研究人员了解疾病的病理 | |
| D. | 意大利化学家阿伏伽德罗提出了原子学说,为近代化学的发展奠定了基础 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在放电时,正极发生的反应是Pb(s)+SO42-(aq)-2e-═PbSO4(s) | |
| B. | 在放电时,该电池的负极材料是铅板 | |
| C. | 在充电时,电池中硫酸的浓度不断变小 | |
| D. | 在充电时,阳极发生的反应是PbSO4(s)+2e-═Pb(s)+SO42-(aq) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com