
分析 有A、B、C三种有机物,A是一种环状烃,其中碳、氢两种元素的质量比为6:1,则A中C、H原子物质的量之比=A中n(C):n(H)=$\frac{6}{12}$:$\frac{1}{1}$=1:2,故A的实验式为CH2;
气体A的质量是相同状况下同体积空气质量的1.448倍,则M(A)=1.448×29=42,设A的分子式为(CH2)n,计算n值,从而确定分子式;
B是A的同分异构体,能使酸性高锰酸钾溶液退色,说明B中含有碳碳不饱和键,
B跟溴水反应生成C溴代烃,据此写出 A、B、C的结构简式.
解答 解:有A、B、C三种有机物,A是一种环状烃,其中碳、氢两种元素的质量比为6:1,则A中C、H原子物质的量之比=A中n(C):n(H)=$\frac{6}{12}$:$\frac{1}{1}$=1:2,故A的实验式为CH2;
设A的分子式为(CH2)n,则n=$\frac{42}{14}$=3,A的分子式为C3H6,
A是一种环状烃,则A结构简式为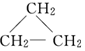 ;
;
B是A的同分异构体,能使酸性高锰酸钾溶液退色,说明B中含有碳碳不饱和键,则B结构简式为CH3-CH═CH2,
B跟溴水反应生成C为溴代烃,C结构简式为CH3-CHBrCH2Br,
答:A、B、C结构简式分别为 、CH3-CH═CH2、CH3-CHBrCH2Br.
、CH3-CH═CH2、CH3-CHBrCH2Br.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断、计算能力,正确判断A分子式是解本题关键,知道物质之间的转化、物质分子组成特点即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1mol CO(g)和1molH2O(g)充分反应,放出的热量为aKJ | |
| B. | 改变压强,平衡不发生移动,反应放出的热量不变 | |
| C. | 升高温度,速率加快,反应放出的热量不变 | |
| D. | 若将该反应设计为原电池,反应放出的热量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 构成原电池的正极和负极必须是两种不同的金属 | |
| B. | 任何化学反应只要是自发进行的放热反应都可以被设计成原电池 | |
| C. | 在原电池中,电子流出的一极是负极,该电极被还原 | |
| D. | 原电池是化学能转变为电能的装置,为外界提供电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | 单质在自然界中硬度最大 |
| B | 原子中s能级与p能级电子数相等且有单电子 |
| C | C在B的下一周期,C的电离能数据(kJ•mol-1)为:I1=738I2=1451I3=7732I4=10540 |
| D | 单质密度小,较好的延展性,广泛用于食品包装,D的氧化物是两性氧化物 |
| E | 单质是一种常见金属,与B元素能形成黑色和砖红色两种氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液中存在的离子只有Cl-、OH-、NH4+、H+,该溶液中离子浓度大小关系可能为:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 0.1mol•L-1(NH4)2SO4溶液中:c(H+)>c(NH4+) | |
| C. | 0.1mol•L-1的HCl溶液与0.1mol•L-1的NaOH溶液等体积混合:c(H+)+c(Na+)═c(OH-)+c(Cl-) | |
| D. | 0.1mol•L-1 CH3COONa溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 空气、Cl2 | B. | NaHCO3、蔗糖 | C. | Ba(OH)2、CH3CH2OH | D. | H2SO4、盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径的大小顺序为 W>Q>Z>X>Y | |
| B. | 元素 Y 与 W 对应氢化物的沸点 H2Y>H2W | |
| C. | 元素 X 与 Y 可以形成 5 种以上的化合物 | |
| D. | 元素 Q 的最高价氧化物对应的水化物酸性比 W 的强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com