
| A. | C2H5Cl→CH2=CH2 | B. | 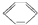 → → | ||
| C. | CH≡CH→CH2=CH2 | D. | CH3COOH→CH3COOC2H5 |
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
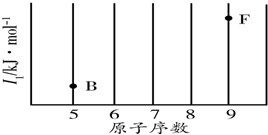 研究物质的微观结构,有助于人们理解物质变化的本质.请回答下列问题.
研究物质的微观结构,有助于人们理解物质变化的本质.请回答下列问题.| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阴极增重1.4g | B. | 所得溶液pH<1 | C. | 阴极增重0.64g | D. | 所得溶液pH>1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
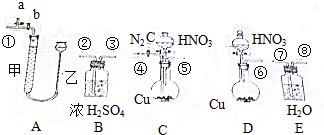
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2 | B. | CO2 | C. | C2H6O | D. | H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 自然界中有11H、12H、13H三种氢的同位素,它们的化学性质不相同 | |
| B. | ${\;}_{1}^{1}$H失去1个电子后,变成1个质子 | |
| C. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H是三种不同的原子 | |
| D. | 11H、21H、31H在化学反应中容易失去一个电子而显+1价 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 工业合成氨是利用氮气和氢气在一定条件下反应生成的.氨是重要的工业原料.请回答下列问题:
工业合成氨是利用氮气和氢气在一定条件下反应生成的.氨是重要的工业原料.请回答下列问题: ;
; ;指出分子中化学键是共价键(填‘离子键’或‘共价键’).
;指出分子中化学键是共价键(填‘离子键’或‘共价键’).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯与氯气加成(1,2-二氯乙烷) | |
| B. | 等物质的量的氯气与乙烷在光照下反应(氯乙烷) | |
| C. | 乙烯与水加成(乙醇) | |
| D. | 乙烯与氯化氢在一定条件下反应(氯乙烯) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com