
ijӊ»śĪļXµÄ·Ö×ÓŹ½ĪŖC3H6O2£®XŌŚĖįŠŌĢõ¼žĻĀÓėĖ®·“Ó¦£¬Éś³ÉµÄÓŠ»śĪļYŗĶZ£®YŌŚĶ“ß»ÆĻĀ±»Ńõ»ÆĪŖW£¬ZŗĶWÄÜ·¢ÉśŅų¾µ·“Ó¦£®
£Ø1£©XŗĶZµÄĆū³ĘĪŖ£ŗX””””£¬Z””””£®
£Ø2£©Š“³öĻĀĮŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
YÓėÅØĮņĖįµÄ»ģŗĻĪļ¹²ČČ·¢ÉśĻūČ„·“Ó¦””””£¬WÓėŠĀÖĘCu£ØOH£©2”¢NaOH»ģŗĻČÜŅŗ¹²ČČ·¢ÉśµÄ·“Ó¦””””£®
| ÓŠ»śĪļŹµŃéŹ½ŗĶ·Ö×ÓŹ½µÄČ·¶Ø£® | |
| ×ØĢā£ŗ | ÓŠ»śĪļµÄ»ÆѧŠŌÖŹ¼°ĶʶĻ£® |
| ·ÖĪö£ŗ | ijӊ»śĪļXµÄ·Ö×ÓŹ½ĪŖC3H6O2£®XŌŚĖįŠŌĢõ¼žĻĀÓėĖ®·“Ó¦£¬Éś³ÉµÄÓŠ»śĪļYŗĶZ£®YŌŚĶ“ß»ÆĻĀ±»Ńõ»ÆĪŖW£¬ZŗĶWÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ŌņZĪŖ¼×Ėį£¬YĪŖŅŅ“¼£¬WÄÜŅŅČ©£¬Č»ŗóøł¾ŻĪļÖŹµÄŠŌÖŹĄ“ŹéŠ“·½³ĢŹ½£» |
| ½ā“š£ŗ | ½ā£ŗijӊ»śĪļXµÄ·Ö×ÓŹ½ĪŖC3H6O2£®XŌŚĖįŠŌĢõ¼žĻĀÓėĖ®·“Ó¦£¬Éś³ÉµÄÓŠ»śĪļYŗĶZ£®YŌŚĶ“ß»ÆĻĀ±»Ńõ»ÆĪŖW£¬ZŗĶWÄÜ·¢ÉśŅų¾µ·“Ó¦£¬ŌņXĪŖ¼×Ėįõ„£¬ZĪŖ¼×Ėį£¬YĪŖŅŅ“¼£¬WÄÜŅŅČ©£¬ŅŅ“¼ŗĶÅØĮņĖį¹²Čȵ½1700CŹ±·¢ÉśĻūČ„·“Ó¦£¬Éś³ÉŅŅĻ©£¬·½³ĢŹ½ĪŖ£ŗC2H5OH ¹Ź“š°øĪŖ£ŗ£Ø1£©¼×ĖįŅŅõ„£»¼×Ėį£» £Ø2£©C2H5OH |
| µćĘĄ£ŗ | ±¾Ģā×¢Ņāæ¼²éĮĖÓŠ»śĪļµÄŠŌÖŹ£¬×¢ŅāÓŠ»śĪļµÄĶʵ¼ŹĒ½āĢāµÄ¹Ų¼ü£¬ÄŃ¶Č²»“ó£® |
””


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
»ÆѧÓėÉē»į”¢Éś²ś”¢Éś»īĆÜĒŠĻą¹Ų”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
(””””)
A.ŹÆÓ¢Ö»ÄÜÓĆÓŚÉś²ś¹āµ¼ĻĖĪ¬
B.“Óŗ£Ė®ÖŠĢįČ”ĪļÖŹ¶¼±ŲŠėĶعż»Æѧ·“Ó¦²ÅÄÜŹµĻÖ
C.ĪŖĮĖŌö¼ÓŹ³ĪļµÄÓŖŃų³É·Ö,æÉŅŌ“óĮæŹ¹ÓĆŹ³Ę·Ģķ¼Ó¼Į
D.”°µŲ¹µÓĶ”±½ūÖ¹Ź³ÓĆ,µ«æÉŅŌÓĆĄ“ÖĘ·ŹŌķ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚĻĀĮŠ·“Ó¦ÖŠ£¬aXO4﹣+bY﹣+cH+═dX2++eY2+8H2O£¬»Æѧ¼ĘĮæŹżb£¬d·Ö±šĪŖ£Ø””””£©
| ”” | A£® | 5£¬6 | B£® | 10£¬2 | C£® | 6£¬2 | D£® | 10£¬5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓÉŅŅĻ©ŗĶŅŅ“¼ÕōĘū×é³ÉµÄ»ģŗĻĘųĢåÖŠ£¬ČōĢ¼ŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ72%£¬ŌņŃõŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ£Ø””””£©
| ”” | A£® | 32.00% | B£® | 16.00% | C£® | 14.22% | D£® | 2.14% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Į½ÖÖĘųĢ¬ĢžŅŌŅ»¶Ø±ČĄż»ģŗĻ£¬ŌŚ105”ꏱ1LøĆ»ģŗĻĢžÓė9LŃõĘų»ģŗĻ£¬³ä·ÖČ¼ÉÕŗó»Öø“µ½ŌדĢ¬£¬ĖłµĆĘųĢåĢå»żČŌŹĒ10L£®ĻĀĮŠø÷×é»ģŗĻĢžÖŠ²»·ūŗĻ“ĖĢõ¼žµÄŹĒ£Ø””””£©
| ”” | A£® | CH4 C2H4 | B£® | CH4 C3H6 | C£® | C2H4 C3H4 | D£® | C2H2 C3H6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚĢå»żæɱäµÄČŻĘ÷ÖŠ·¢Éś·“Ó¦N2+3H2⇌NH3µ±Ōö“óŃ¹ĒæŹ¹ČŻĘ÷Ģå»żĖõŠ”Ź±£¬»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ£¬ĘäÖ÷ŅŖŌŅņŹĒ£Ø””””£©
| ”” | A£® | ·Ö×ÓŌĖ¶ÆĖŁĀŹ¼Óæģ£¬Ź¹·“Ó¦Īļ·Ö×Ó¼äµÄÅöײ»ś»įŌö¶ą |
| ”” | B£® | ·“Ó¦Īļ·Ö×ÓµÄÄÜĮæŌö¼Ó£¬»ī»Æ·Ö×Ó°Ł·ÖŹżŌö“ó£¬ÓŠŠ§Åöײ“ĪŹżŌö¶ą |
| ”” | C£® | »ī»Æ·Ö×Ó°Ł·ÖŹżĪ“±ä£¬µ«µ„Ī»Ģå»żÄŚ»ī»Æ·Ö×ÓŹżŌö¼Ó£¬ÓŠŠ§Åöײ“ĪŹżŌö¶ą |
| ”” | D£® | ·Ö×Ó¼ä¾ąĄė¼õŠ”£¬Ź¹ĖłÓŠµÄ»ī»Æ·Ö×Ó¼äµÄÅöײ¶¼³ÉĪŖÓŠŠ§Åöײ |
| ”” | D£® | ·Ö×Ó¼ä¾ąĄė¼õŠ”£¬Ź¹ĖłÓŠµÄ»ī»Æ·Ö×Ó¼äµÄÅöײ¶¼³ÉĪŖÓŠŠ§Åöײ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
25”ęŗĶ1.01”Į105PaŹ±£¬·“Ó¦2N2O5£Øg£©=4NO2£Øg£©+O2£Øg£©”÷H=+56.76kJ/mol£¬×Ō·¢½ųŠŠµÄŌŅņŹĒ£Ø””””£©
| ”” | A£® | ŹĒĪüČČ·“Ó¦ | B£® | ŹĒ·ÅČČ·“Ó¦ |
| ”” | C£® | ŹĒģŲ¼õÉŁµÄ·“Ó¦ | D£® | ģŲŌö“óŠ§Ó¦“óÓŚÄÜĮ抧Ӧ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
µŖŹĒµŲĒņÉĻŗ¬Įæ·įø»µÄŅ»ÖÖŌŖĖŲ£¬µŖ¼°Ęä»ÆŗĻĪļŌŚ¹¤Å©ŅµÉś²ś”¢Éś»īÖŠÓŠ×ÅÖŲŅŖ×÷ÓĆ£¬
£Ø1£©ČēĶ¼ŹĒN2£Øg£©ŗĶH2£Øg£©·“Ӧɜ³É1mol NH3£Øg£©¹ż³ĢÖŠÄÜĮæ±ä»ÆŹ¾ŅāĶ¼£¬ĒėŠ“³öN2ŗĶH2·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£ŗ””””£»
£Ø2£©ČōŅŃÖŖĻĀĮŠŹż¾Ż£ŗ
| »Æѧ¼ü | H﹣H | N”ŌN |
| ¼üÄÜ/kJ•mol﹣1 | 435 | 943 |
ŹŌøł¾Ż±ķÖŠ¼°Ķ¼ÖŠŹż¾Ż¼ĘĖćN﹣HµÄ¼üÄÜ””””kJ•mol﹣1
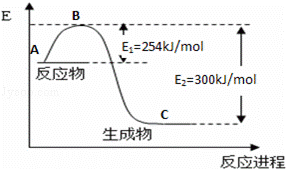
£Ø3£©ŗĻ³É°±·“Ó¦Ķس£ÓĆĢś“„Ć½×÷“߻ƼĮ£®Ź¹ÓĆĢś“„Ć½ŗóE1ŗĶE2µÄ±ä»ÆŹĒ£ŗE1””””£¬E2””£ØĢī”°Ōö“ó”±”¢”°¼õŠ””¢”±”°²»±ä”±£©£®
£Ø4£©ÓĆNH3“߻ƻ¹ŌNOX»¹æÉŅŌĻū³żµŖŃõ»ÆĪļµÄĪŪČ¾£®ĄżČē
4NH3£Øg£©+3O2£Øg£©=2N2£Øg£©+6H2O£Øg£©£»”÷H1=akJ/mol
N2£Øg£©+O2£Øg£©=2NO£Øg£©£»”÷H2=bkJ/mol
Čō1mol NH3»¹ŌNOÖĮN2£¬ŌņøĆ·“Ó¦¹ż³ĢÖŠµÄ·“Ó¦ČČ”÷H3=””””kJ/mol£ØÓĆŗ¬a”¢bµÄŹ½×Ó±ķŹ¾£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆCOŗĶH2ŗĻ³ÉCH3OHµÄ»Æѧ·½³ĢŹ½ĪŖCO£Øg£©+2H2£Øg£©═CH3OH£Øg£©”÷H£¼0£¬°“ÕÕĻąĶ¬µÄĪļÖŹµÄĮæĶ¶ĮĻ£¬²āµĆCOŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄĘ½ŗā×Ŗ»ÆĀŹÓėŃ¹ĒæµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
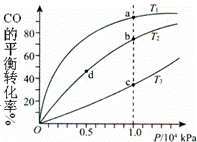
| ”” | A£® | ĪĀ¶Č£ŗT1£¾T2£¾T3 |
| ”” | B£® | Õż·“Ó¦ĖŁĀŹ£ŗ¦Ō£Øa£©£¾¦Ō£Øc£© ¦Ō£Øb£©£¾¦Ō£Ød£© |
| ”” | C£® | Ę½ŗā³£Źż£ŗK£Øa£©£¾K£Øc£© K£Øb£©=K£Ød£© |
| ”” | D£® | Ę½¾łÄ¦¶ūÖŹĮæ£ŗM£Øa£©£¼M£Øc£© M£Øb£©£¼M£Ød£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com