
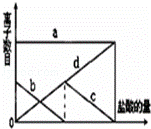
少量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生如图变化.四条曲线(c和d图象部分重叠)溶液中离子的对应关系,正确的是( )
|
| A. | a:Cl﹣b:K+ c:CO32﹣ d:HCO3﹣ |
|
| B. | a:K+ b:CO32﹣ c:Cl﹣ d:HCO3﹣ |
|
| C. | a:K+ b:CO32﹣ c:HCO3﹣ d:Cl﹣ |
|
| D. | a:K+b:HCO3﹣ c:Cl﹣ d:CO32﹣ |
| 离子浓度大小的比较;离子方程式的有关计算. | |
| 专题: | 离子反应专题. |
| 分析: | 根据向一定量的K2CO3溶液中缓慢地滴加稀盐酸,则先后发生K2CO3+HCl═KCl+KHCO3、KHCO3+HCl═KCl+CO2↑+H2O,则钾离子数目不发生变化,氯离子的数目在增加,碳酸根离子的数目一直在减少,直到为0,碳酸氢根离子的数目先增大后减小,直到为0,然后结合图象来分析对应的离子. |
| 解答: | 解:因向一定量的K2CO3溶液中缓慢地滴加稀盐酸,先后发生如下反应, K2CO3+HCl═KCl+KHCO3、KHCO3+HCl═KCl+CO2↑+H2O, 则钾离子的数目不变,即图中a为K+离子, 碳酸根离子在减少,直至为0,即图中b为CO32﹣离子, 碳酸氢根离子先增大后减小,直至为0,即图中c为HCO3﹣离子, 氯离子先为0,随盐酸的加入氯离子的数目在增多,即图中d为Cl﹣离子, 故选C. |
| 点评: | 本题以碳酸盐与盐酸的反应及图象考查离子浓度大小的比较,为高频考点,把握发生的反应及反应与图象的对应关系为解答的关键,侧重分析与应用能力的考查,题目难度不大. |


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
下列各组中的反应,属于同一反应类型的是( )
A.乙烯水化制乙醇;乙烷光照条件下制取溴乙烷
B.甲苯使酸性高锰酸钾溶液褪色;丙炔和氢气反应制取丙烷
C.甲苯硝化制TNT;乙炔与氯化氢反应制氯乙烯
D.由苯制溴苯;由乙酸与乙醇反应制乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式中正确的是( )
A. 钠与水反应:2Na+2H2O=2Na++2OH﹣+H2↑
B. 氢氧化钡溶液和硫酸铵溶液反应:Ba2++SO42﹣=BaSO4↓
C. 硫化钠溶于水呈碱性:S2﹣+2H2O⇌H2S+2OH﹣
D. 向溴化亚铁溶液中通入少量氯气:Cl2+2Br﹣=2Cl﹣+Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中能大量共存的是( )
|
| A. | Fe3+、SCN﹣、Na+、Cl﹣ | B. | Cl﹣、AlO2﹣、HCO3﹣、Na+ |
|
| C. | Fe2+、NH4+、SO42﹣、S2﹣ | D. | Ca2+、HCO3﹣、Cl﹣、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量的锌与100mL 18.5mol•L﹣1浓硫酸充分反应后,锌完全溶解,同时生成气体A 33.6L(标准状况).将反应后的溶液稀释至1L,则得溶液中c(H+)=0.1mol•L﹣1,则下列叙述中错误的是( )
|
| A. | 气体A为SO2和H2的混合物 | B. | 气体A中SO2和H2的体积比为1:5 |
|
| C. | 反应中消耗的Zn的质量为97.5 g | D. | 反应中共转移电子3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属腐蚀与防护的说法正确的是
A.在铁门上焊接铜块能防腐蚀
B.镀锡铁制品的镀层破损后,镀层仍能对铁制品起保护作用
C.钢柱在水下部分比在空气与水交界处更容易腐蚀
D.在海轮外壳连接锌块,保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
利用催化氧化反应将SO2转化为SO3是工业上生产
硫酸的关键步骤.
(1)T1℃时,在1L密闭容器中充入0.6molSO3,图1表示SO3
物质的量随时间的变化曲线。
①平衡时,SO3的转化率为 (保留小数点后一位) ;
T1℃时,反应2SO2(g)+O2(g)  2SO3(g) 的平衡常数为 ;其他条件不变,在8min时压缩容器体积至0.5L,则n(SO3
2SO3(g) 的平衡常数为 ;其他条件不变,在8min时压缩容器体积至0.5L,则n(SO3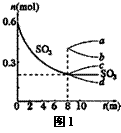 )的变化曲线为 (填字母)。
)的变化曲线为 (填字母)。
②下表为不同温度(T)下,反应2SO2(g)+O2(g)  2SO3(g) (△H<0)的化学平衡常数(K)
2SO3(g) (△H<0)的化学平衡常数(K)
| T/℃ | T2 | T3 |
| K | 20.5 | 4.68 |
由此推知,温度最低的是 (填“T1”、“T2” 或 “T3”)。
③在温度为T1℃时,向该1L的密闭容器中同时加入0.2molSO2、xmolO2、0.2molSO3三种气体,在达到平衡前若要使SO3的浓度减小,则x的取值范围是 。
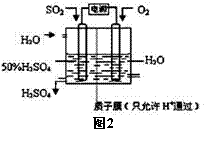
(2)科学家研究出用电化学原理生产硫酸的新工艺,装置如图2所示,总反应的化学方程式为 ,其阳极的电极反应式为
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验时可用推拉注射器活塞
的方法检查右图中装置的气密性。当向外拉活塞时,如果装置气密性良
好,可能观察到

A.长颈漏斗下端管口产生气泡
B.瓶中液面明显上升
C.长颈漏斗内的液面上升
D.注射器内有液体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com